測定鎂帶變質程度.鎂帶久置于空氣中會變質為堿式碳酸鎂,現要測定一表面變質為堿式碳酸鎂的鎂帶的純度,(查閱資料)堿式碳酸鎂能與鹽酸反應生成氯化鎂、水和二氧化碳.(實驗裝置)
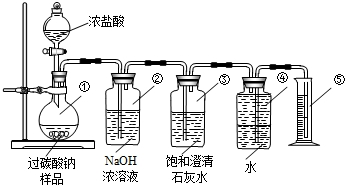
【結論與討論】
Ⅰ.小明同學認為測定產物中H
2的體積既可測定樣品的純度.
(1)裝置②的作用是:
;
(2)裝置③的作用是:
;
(3)判定鎂帶試樣是否完全反應的實驗操作方法和現象是
;
(4)稱取樣品與足量濃硫酸充分反應后,收集到的氫氣體積為0.448L(已知該實驗條件下氫氣的密度為0.089g/L),則稱取的樣品質量應大于
g.
Ⅱ.小江同學認為測定產物中的CO
2的質量(即反應前后裝置②的質量差)也可測定樣品中單質鎂的純度.但利用上述實驗裝置測得CO
2的質量并計算樣品的純度,結果偏低,你認為原因可能是
.
A.濃硫酸易揮發,產生氯化氫氣體被裝置②吸收
B.二氧化碳氣體逸出時帶出水蒸氣在裝置②中冷凝而被吸收
C.裝置①②內空氣中二氧化碳被裝置②吸收
D.實驗結束時燒瓶中殘留二氧化碳
E.氣體從氫氧化鈉溶液中逸出是帶出部分水蒸氣.




 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案