解:(1)草酸(H
2C
2O
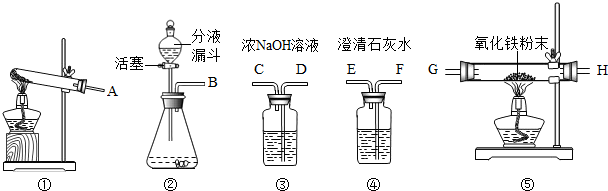
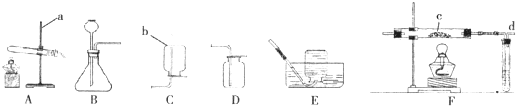
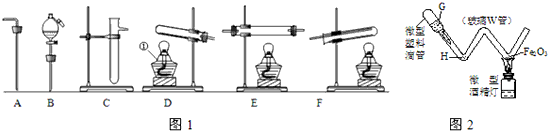
4) 固體在濃硫酸作用下發生反應,若用該反應來制取CO,制氣裝置應選BC,因為是固體與液體反應;二氧化碳氣體一般用澄清的石灰水檢驗,用氫氧化鈉溶液吸收.故答案為:BC;c
(2)一氧化碳具有可燃性,不純時容易引起爆炸,因此使用以前,一定要檢驗一氧化碳的純度.若用CO還原氧化銅粉末,應選裝置E,因為一氧化碳有毒,要進行尾氣處理.一氧化碳和氧化銅在加熱的條件下生成銅和二氧化碳.故答案為:檢驗氫一氧化碳的純度;E;CO+CuO

Cu+CO
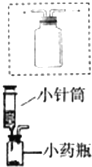
2(3)氫氣還原氧化鐵生成鐵和水,現象是紅色變黑色,微型儀器進行實驗的優點是:節約藥品;產生的廢棄物也很少,污染少等.故答案為:紅色變黑色;F;產生的廢棄物也很少,污染少
(4)設電解的水的質量為x
2H
2O

2H
2↑+O
2↑
36 4
x 1g
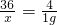
x=9g 答:電解的水的質量是9g.
電解水的過程中硫酸的質量不變=45g×8%=3.6g,
根據質量分數公式,電解后的硫酸溶液的溶質質量分數=
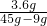
×100%=10%
故答案為:(1)9g;(2)10%
分析:草酸(H
2C
2O
4) 固體在濃硫酸作用下發生反應,若用該反應來制取CO,制氣裝置應選BC,因為是固體與液體反應;二氧化碳氣體一般用澄清的石灰水檢驗,用氫氧化鈉溶液吸收.一氧化碳具有可燃性,不純時容易引起爆炸,因此使用以前,一定要檢驗一氧化碳的純度.若用CO還原氧化銅粉末,應選裝置E,因為一氧化碳有毒,要進行尾氣處理.一氧化碳和氧化銅在加熱的條件下生成銅和二氧化碳.氫氣還原氧化鐵生成鐵和水,現象是紅色變黑色,微型儀器進行實驗的優點是:節約藥品;產生的廢棄物也很少,污染少等.根據化學方程式計算的步驟有:一設、二寫、三找、四列、五答、六查.在本題中,已知氫氣的質量可以求出水的質量;根據質量分數公式,可以求出電解后的硫酸溶液的溶質質量分數.
點評:本考點考查了儀器的選擇、一氧化碳和氫氣的化學性質、化學方程式的書寫以及根據化學方程式的計算,綜合性比較強.有關的計算屬于質量分數和化學方程式的綜合應用,是中考計算題中經常出現的題型.做題時要注意:化學方程式要寫正確,始終不要忘記質量守恒定律.本考點主要出現在計算題中.

 Cu+CO2
Cu+CO2 2H2↑+O2↑
2H2↑+O2↑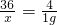 x=9g 答:電解的水的質量是9g.
x=9g 答:電解的水的質量是9g.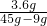 ×100%=10%
×100%=10%

 小博士期末闖關100分系列答案
小博士期末闖關100分系列答案 名校名師培優作業本加核心試卷系列答案
名校名師培優作業本加核心試卷系列答案