
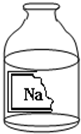
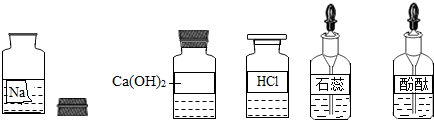
 某校興趣小組同學準備進行常見酸、堿、鹽的性質實驗時,發現實驗臺上擺放的藥品中(如圖),有一裝溶液的試劑瓶未蓋瓶蓋且標簽破損,于是決定對這瓶溶液進行實驗探究:
某校興趣小組同學準備進行常見酸、堿、鹽的性質實驗時,發現實驗臺上擺放的藥品中(如圖),有一裝溶液的試劑瓶未蓋瓶蓋且標簽破損,于是決定對這瓶溶液進行實驗探究:

科目:初中化學 來源: 題型:閱讀理解
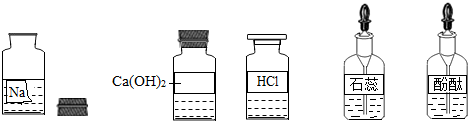
 某校興趣小組同學準備進行常見的酸、堿、鹽的性質實驗時,發現實驗臺上擺放的藥品中有一個裝溶液的試劑瓶未蓋瓶蓋且標簽破損(如圖),于是決定對這瓶溶液進行實驗探究:
某校興趣小組同學準備進行常見的酸、堿、鹽的性質實驗時,發現實驗臺上擺放的藥品中有一個裝溶液的試劑瓶未蓋瓶蓋且標簽破損(如圖),于是決定對這瓶溶液進行實驗探究:查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
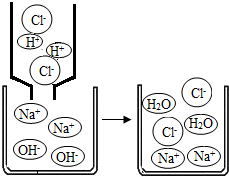
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
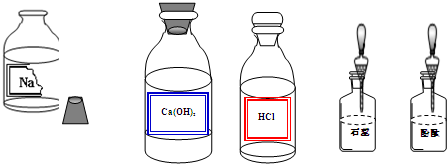
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解

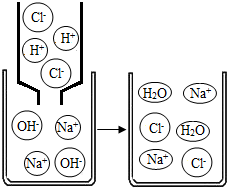
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com