
| A. | 參加反應的氧氣的質量為80g | |
| B. | 反應的化學方程式中CO2和H2O的化學計量數之比為2:1 | |
| C. | 若增加16gO2,甲烷能完全燃燒生成CO2和H2O | |
| D. | X的化學式為CO |
分析 根據質量守恒定律計算參加反應的氧氣的質量;根據 CO2和 H2O 的質量計算化學計量數之比;根據,24g CH4完全燃燒所需氧氣的量計算.
解答 解:A、根據質量守恒定律,參加反應的氧氣的質量為:54g+22g+28g-24g=80g;故正確;
B、化學方程式中 CO2和 H2O 的化學計量數之比為:$\frac{22g}{44}:\frac{54g}{18}$=1:6;故錯誤;
C、設24g CH4完全燃燒所需氧氣的質量為x
CH4+2O2$\frac{\underline{\;點燃\;}}{\;}$CO2+2H2O
16 64
24g x
$\frac{16}{24g}=\frac{64}{x}$
x=96g
故需增加氧氣的質量為:96g-80g=16g,故正確;
D、一定條件下,24gCH4與80gO2恰好完全反應,生成54gH2O、22gCO2和28gX,24gCH4中含有碳元素的質量為:24g×$\frac{12}{16}$=18g,故含有氫元素的質量為:24g-18g=6g;54gH2O中含有氫元素的質量為:54g×$\frac{2}{18}$×100%=6g;22gCO2中含有碳元素的質量為:22g×$\frac{12}{44}$=6g,故X中含有18g-6g=12g的碳,不含有氫元素,含有氧元素的質量為:80g-(54g-6g)-(22g-6g)=16g,故X中碳原子和氧原子的原子個數比為:$\frac{12g}{12}:\frac{16g}{16}$=1:1.故該物質是一氧化碳,故正確;
故選:B.
點評 本題考查學生質量守恒定律的應用以及利用化學反應方程式的計算,并注意計算格式的規范.


科目:初中化學 來源: 題型:推斷題
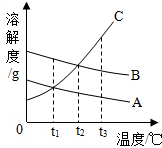 如圖是A、B、C三種固體物質的溶解度曲線,試看圖后回答:
如圖是A、B、C三種固體物質的溶解度曲線,試看圖后回答:查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 三聚氰胺是由15個原子構成 | |
| B. | 三聚氰胺是一種氧化物 | |
| C. | 三聚氰胺的相對分子質量是126 | |
| D. | 三聚氰胺中碳、氮、氫元素的質量比為1:2:2 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 紅磷在空氣中燃燒產生大量的白霧 | |
| B. | 硫在空氣中燃燒發出藍紫色火焰 | |
| C. | 鎂條在氧氣中燃燒發出耀眼的白光、生成黑色固體 | |
| D. | 鐵絲在氧氣中劇烈燃燒,火星四射 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題

| A. | 裝置Ⅱ、Ⅳ組合可制取氧氣 | |
| B. | 裝置Ⅰ可作為固體加熱制取氣體的發生裝置 | |
| C. | 裝置Ⅱ中長頸漏斗可以用分液漏斗、醫用注射器代替 | |
| D. | 裝置Ⅲ、Ⅳ可用于收集密度與空氣密度差距較大,且不與空氣中各成分反應的氣體 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com