
【題目】某興趣小組為測定一包石灰石樣品中碳酸鈣的質量分數,進行實驗:往12克的固體樣品中不斷加入稀鹽酸,直到沒有氣泡產生,共用去稀鹽酸100克。測得相關數據如圖所示: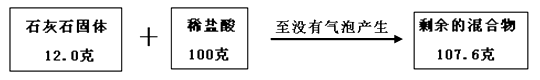
注:①該反應中,樣品中的雜質不參加反應,碳酸鈣完全反應。
②計算結果保留一位小數。
(1)根據質量守恒定律,反應生成二氧化碳的質量為g.
(2)計算該樣品中碳酸鈣的質量分數.(寫出計算過程)
【答案】
(1)4.4g
(2)解:根據質量守恒定律,反應前后物質的總質量不變,生成二氧化碳的質量為100g+12.0g107.6g=4.4g;設樣品中碳酸鈣的質量為x,則
CaCO3+ | 2HCl═ | CaCl2+H2O+ | CO2↑ |
100 | 44 | ||
x | 4.4g |
100/x=44/4.4g x=10g
樣品中碳酸鈣的含量為10g÷12.0g×100%≈83.3%
答:該樣品中碳酸鈣的質量分數為83.3%
【解析】根據質量守恒定律即可算出二氧化碳的質量,再根據二氧化碳的質量即可算碳酸鈣的質量。
故答案為:解:根據質量守恒定律,反應前后物質的總質量不變,生成二氧化碳的質量為100g+12.0g107.6g=4.4g;
設樣品中碳酸鈣的質量為x,則
CaCO3+ | 2HCl═ | CaCl2+H2O+ | CO2↑ |
100 | 44 | ||
x | 4.4g |
100/x=44/4.4g x=10g
樣品中碳酸鈣的含量為10g÷12.0g×100%≈83.3%
答:該樣品中碳酸鈣的質量分數為83.3%
本題主要考察質量守恒定律和依據化學方程式的計算。在化學反應中,參加反應的物質質量等于新生產的物質質量,而且各物質質量之比等于相對分子質量乘以化學計量數之比。


科目:初中化學 來源: 題型:
【題目】合肥市某中學化學興趣小組按照課本實驗方法 ,做木炭與氧化銅反應實驗時,發現很難觀察到紫紅色銅的生成,卻往往有暗紅色固體出現。他們決定對這個實驗進行探究和改進。

【提出問題】暗紅色的固體是什么?如何選擇合適的條件,使木炭還原氧化銅的實驗現象更明顯?
【查閱資料】銅有+1和+2兩種化合價,通常情況下,氧的化合價為-2,碳的化合價為+4或-4。
【猜想與假設】
(1)同學們認為這種暗紅色固體可能是一種化合物,并猜測它的化學式為__________________。
(2)同學們還認為,通過改變反應物的狀態、質量比,以及反應裝置,可以使該實驗現象更加明顯,減少出現暗紅色固體的情況。
【分析與交流】
(1)小吳建議用超細炭粉與氧化銅粉末進行實驗。你認為這樣建議的原理是__________________________________________________。
(2)小周建議用圖中的乙裝置替代甲裝置。與甲相比較,乙裝置中將試管直立放置的作用是__________________________________________。
(3)對下列三種氧化銅和碳的質量比例,小施建議選擇___________(填選項序號)的比例。
A. 32︰3 B. 40︰3 C. 48︰3
你認為小施這樣選擇的理由是__________________________________________________。
【實驗與結論】
同學們決定按改進后的方案進行實驗,他們在檢驗了乙裝置的__________后,往試管中加入已干燥的藥品并開始加熱,當看到澄清的石灰水剛出現渾濁時,________(填“可以”或“不能”)確定氧化銅和炭粉已經開始反應。
不久,即可看到試管底部變紅熱,停止加熱后,仍能看到紅熱現象,并沿試管底部自下而上蔓延,這個現象說明該反應是________(填“吸”或“放”)熱反應。
待反應結束,先將導氣管從石灰水中取出,然后關閉止水夾,讓產物自然冷卻。若不關閉止水夾,可能出現的問題是____________________________________________。
待產物冷卻后,同學們終于找到了期待已久的紫紅色銅珠,實驗獲得了圓滿成功。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列關于實驗現象描述正確的是
A.鎂帶在空氣中燃燒,放出耀眼的白光,生成白色固體氧化鎂
B.磷在空氣中燃燒,產生大量白色煙霧
C.鐵絲在氧氣中劇烈燃燒,火星四射,生成黑色固體物質
D.氫氣在空氣中燃燒發出黃色火焰
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】2019年3月22日第二十七屆“世界水日”的宣傳主題為“ Leaving no one behind”(不讓任何一個人掉隊)。下列有關說法不正確的是( )
A.目前世界面臨缺水危機
B.減少盆浴次數,控制水量
C.地球上海水可以直接飲用
D.綜合利用滴灌技術,發展節水農業
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】硒是人體必需的微量元素,圖1是元素周期表中硒元素的信息,圖2是硒原子的結構示意圖,回答下列問題。

(1)硒元素在元素周期表中位于第________周期。
(2)硒元素屬于________(填“金屬”或“非金屬”)元素,其原子核外有_____個電子層。
(3)在元素周期表中,硒元素所在族的第一個元素對應原子在化學反應中容易________(填“得到”或“失去”)電子形成離子,該離子的化學符號為________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com