
Cu與Zn的合金稱為黃銅,有優良的導熱性和耐腐蝕性,可用于制作各種儀器零件。某化學興趣小組的同學為了測定某黃銅的組成,取20g該黃銅樣品于燒杯中,向其中分5次加入相同溶質質量分數的稀硫酸,使之充分反應。每次所用稀硫酸的質量及剩余固體的質量記錄于下表:
| | 加入稀硫酸的質量(g) | 充分反應后剩余固體的質量(g) |
| 第1次 | 20 | 17.4 |
| 第2次 | 20 | 14.8 |
| 第3次 | 20 | 12.2 |
| 第4次 | 20 | 12.0 |
| 第5次 | 20 | m |
(1)12 (1分) (2)40% (2分)(3)19.6%
解析試題分析:(1)由表中數據可知,每加入20g稀硫酸,都將反應2.6g鋅,到第4次的時候,固體只減少了0.2g,說明此時鋅已經全部反應完了,故第5次加入硫酸,固體質量不會改變,所以m=12g。
(2)黃銅樣品中鋅的質量分數為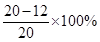 =40%;
=40%;
(3)與20g稀硫酸完全反應的鋅的質量 = 20g-17.4g=2.6g
解:設,20g稀硫酸中H2SO4的質量為x。
Zn + H2SO4 = ZnSO4 + H2↑
65 98
2.6g x 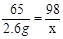
x=3.92g
所用稀硫酸中溶質的質量分數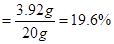
考點:溶液中溶質的質量分數;根據化學方程是計算。
點評:根據化學方程式計算,要注意解題的步驟,設、寫、找、列、解、答。
溶質質量分數= 。
。


 科學實驗活動冊系列答案
科學實驗活動冊系列答案科目:初中化學 來源: 題型:
| 第一次 | 第二次 | 第三次 | |
| 加入稀硫酸的質量(g) | 50 | 50 | 50 |
| 生成氫氣的質量(g) | 0.4 | m | 0.2 |
查看答案和解析>>
科目:初中化學 來源: 題型:
 (2013?浦口區一模)Cu與Zn的合金稱為黃銅,有優良的導熱性和耐腐蝕性,可用作各種儀器零件.
(2013?浦口區一模)Cu與Zn的合金稱為黃銅,有優良的導熱性和耐腐蝕性,可用作各種儀器零件.| 合金的質量/g | 稀硫酸的體積/mL | 生成氫氣的體積/mL | |
| 第一次 | 2 | 15 | 44.4 |
| 第二次 | 2 | 20 | 44.4 |
| 第三次 | 4 | 15 | 44.4 |
查看答案和解析>>
科目:初中化學 來源: 題型:
| 加入稀硫酸的質量(g) | 充分反應后剩余固體的質量(g) | |
| 第1次 | 40 | m |
| 第2次 | 40 | 14.8 |
| 第3次 | 40 | 12.2 |
| 第4次 | 40 | 11.2 |
| 第5次 | 40 | 11.2 |
查看答案和解析>>
科目:初中化學 來源: 題型:

| 合金的質量/g | 稀硫酸的體積/mL | 生成氫氣的質量/g | |
| 第1次 | 2 | 15 | 0.04 |
| 第2次 | 2 | 20 | 0.04 |
| 第3次 | 4 | 15 | 0.04 |
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com