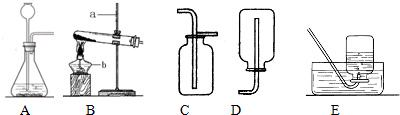
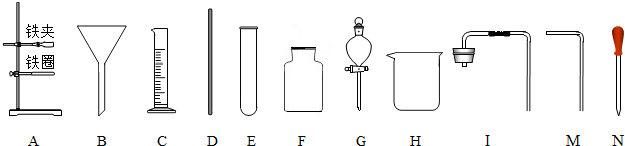
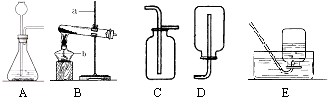
解:(1)a是錐形瓶;b是水槽;
(2)實驗室用氯酸鉀和二氧化錳混合產生氧氣的發生裝置的特點屬于固體加熱型的B裝置,該反應的化學方程式為:2KClO
3
2KCl+3O
2↑;其中二氧化錳起催化作用;
用排水法收集時,為收集到較純的氣體,應該等到氣泡連續均勻冒出時收集;
(3)實驗室制取二氧化碳氣體選用的發生裝置的特點屬于固體和液體常溫下制備氣體,所以發生裝置選擇A;
二氧化碳氣體的密度大于空氣,所以可用向上排空氣法收集,選擇裝置C,因為其溶于水,不能采用排水法收集;
碳酸鈣和鹽酸常溫下反應生成氯化鈣、二氧化碳氣體和水,發生反應的化學方程式為:CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;
(4)“磨砂”是增加玻璃儀器密封性因此集氣瓶用到“磨砂”工藝處理;此外常用到“磨砂”工藝處理的玻璃儀器有:分液漏斗、細口瓶、廣口瓶、滴瓶等;
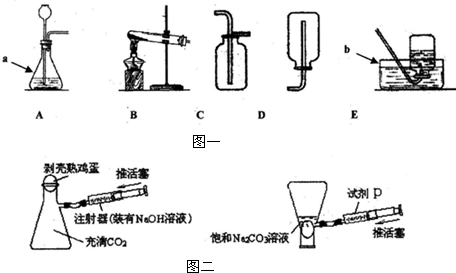
(5)因為二氧化碳被氫氧化鈉溶液吸收后,瓶內壓強減小,在外界大氣壓的作用下,雞蛋進入瓶內;二氧化碳和氫氧化鈉溶液反應的化學方程式為:2NaOH+CO
2=Na
2CO
3+H
2O.
故答案為:(1)錐形瓶;水槽;
(2)B;2KClO
3
2KCl+3O
2↑;催化;氣泡連續均勻冒出時;
(3)A和C;CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;
(4)集氣瓶;
(5)2NaOH+CO
2=Na
2CO
3+H
2O
分析:(1)熟練掌握常見的化學儀器名稱及用途;
(2)根據反應物的狀態和反應條件選擇發生裝置;實驗室用氯酸鉀和二氧化錳混合產生氯化鉀和氧氣,其中二氧化錳起到催化作用;用排水法收集時,為收集到較純的氣體,應該等到氣泡連續均勻冒出時收集;
(3)根據反應物的狀態和反應條件選擇發生裝置,根據氣體的溶解性和密度選擇合適的收集方法;碳酸鈣和鹽酸常溫下反應生成氯化鈣、二氧化碳氣體和水;其中二氧化錳起催化作用;
(4)根據“磨砂”是增加玻璃儀器密封性的一種處理工藝分析;
(5)根據大氣壓不變,瓶內壓強的改變引起的瓶內外壓強差來解釋有關現象.
點評:本題主要考查學生對實驗室制備氧氣和二氧化碳的反應原理、發生裝置的選擇、收集裝置的選擇及有關氣體性質的掌握情況.在分析“瓶吞雞蛋”的魔術時,要根據大氣壓不變,瓶內壓強的改變引起的瓶內外壓強差來解釋有關現象.

 2KCl+3O2↑;其中二氧化錳起催化作用;
2KCl+3O2↑;其中二氧化錳起催化作用; 2KCl+3O2↑;催化;氣泡連續均勻冒出時;
2KCl+3O2↑;催化;氣泡連續均勻冒出時;

 小學課時作業全通練案系列答案
小學課時作業全通練案系列答案