
| A. | 甲>乙>丙>丁 | B. | 乙>甲>丙>丁 | C. | 丁>丙>乙>甲 | D. | 乙>甲>丁>丙 |
 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:解答題
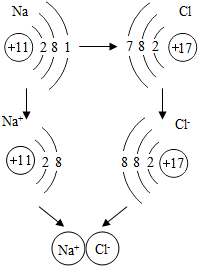 如圖是金屬鈉與氯氣反應生成氯化鈉的微觀示意圖,根據圖示回答下列問題.
如圖是金屬鈉與氯氣反應生成氯化鈉的微觀示意圖,根據圖示回答下列問題.查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
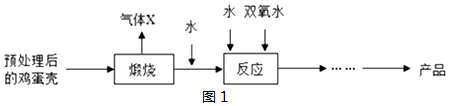
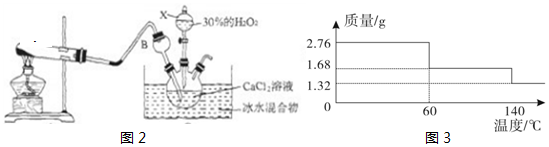
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
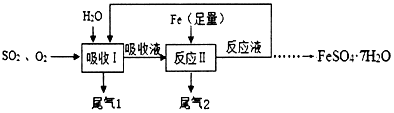
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | NaCl、CaCl2 | B. | Ca(NO3)2Mg(NO3)2 | C. | NaCl Ca(OH)2 | D. | CaCl2MgCO3 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com