
分析 首先根據反應原理找出反應物、生成物、反應條件,根據化學方程式的書寫方法、步驟(寫、配、注、等)進行書寫即可.
解答 解:(1)碳酸鈣在高溫下生成氧化鈣和二氧化碳,反應的化學方程式為:CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaO+CO2↑;該反應符合“一變多”的特征,屬于分解反應;
(2)小蘇打與鹽酸反應生成氯化鈉、水和二氧化碳,反應的化學方程式是NaHCO3+HCl=NaCl+H2O+CO2↑;可用于治療胃酸過多;
(3)工業上用一氧化碳還原氧化鐵煉鐵,主要是利用CO的還原性,在高溫下和氧化鐵反應生成鐵和二氧化碳,反應的化學方程式
為Fe2O3+3CO$\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2;
(4)氨水與硫酸反應生成硫酸銨和水,反應的化學方程式是2NH3•H2O+H2SO4═(NH4)2SO4+2H2O;該反應是兩種化合物相互交換成分生成兩種新的化合物的反應,屬于復分解反應;
(5)鐵絲在氧氣中劇烈燃燒,火星四射,放出大量的熱,生成黑色固體四氧化三鐵,集氣瓶底要放少量的水或細砂,目的是防止降落的熔化物炸裂瓶底.其化學反應方程式是:3Fe+2O2$\frac{\underline{\;點燃\;}}{\;}$Fe3O4;
(6)鐵銹的主要成分是氧化鐵,硫酸和氧化鐵反應生成硫酸鐵和水,故化學方程式為:3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;溶液的顏色會變成黃色;
(7)高錳酸鉀在加熱條件下生成錳酸鉀、二氧化錳和氧氣,反應的化學方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;由于反應后氧氣逸出,完全反應后,固體混合物中錳元素的質量和原來相比變大.
故答案為:(1)CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaO+CO2↑;分解反應;(2)NaHCO3+HCl=NaCl+H2O+CO2↑;治療胃酸過多;(3)Fe2O3+3CO$\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2;(4)2NH3•H2O+H2SO4═(NH4)2SO4+2H2O;復分解反應;(5)3Fe+2O2$\frac{\underline{\;點燃\;}}{\;}$Fe3O4;防止降落的熔化物炸裂瓶底;(6)3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;黃色;
(7)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;變大
點評 本題難度不大,考查學生根據反應原理書寫化學方程式的能力,化學方程式書寫經常出現的錯誤有不符合客觀事實、不遵守質量守恒定律、不寫條件、不標符號等.


 暑假作業海燕出版社系列答案
暑假作業海燕出版社系列答案 本土教輔贏在暑假高效假期總復習云南科技出版社系列答案
本土教輔贏在暑假高效假期總復習云南科技出版社系列答案 暑假作業北京藝術與科學電子出版社系列答案
暑假作業北京藝術與科學電子出版社系列答案科目:初中化學 來源: 題型:選擇題
| A. | 置換反應生成單質和化合物,生成單質和化合物的反應一定是置換反應 | |
| B. | 單質中只含有一種元素,只含有一種元素的物質一定是單質 | |
| C. | 化合物是不同種元素組成的純凈物,不同種元素組成的純凈物一定是化合物 | |
| D. | 活潑金屬能與稀酸反應放出氣體,能與稀酸反應放出氣體的一定是活潑金屬 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 碳酸鈉 純堿 Na2CO3 | B. | 氫氧化鈣 石灰石 Ca(OH)2 | ||
| C. | 氧化鈣 生石灰 CaO | D. | 氫氧化鈉 火堿 NaOH |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 洗潔精能溶解油污 | |
| B. | 溶液上層的密度小,下層的密度大 | |
| C. | 固體、液體或氣體都可以作為溶質 | |
| D. | 燒堿溶液和蔗糖溶液都具有很強的導電性 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
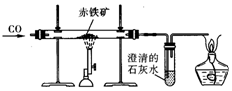 小文同學利用下圖實驗裝置測定某赤鐵礦石樣品中Fe2O3的質量分數,取10g樣品與足量CO充分反應后,測得剩余固體的質量為7.6g,下列說法正確的是( )
小文同學利用下圖實驗裝置測定某赤鐵礦石樣品中Fe2O3的質量分數,取10g樣品與足量CO充分反應后,測得剩余固體的質量為7.6g,下列說法正確的是( )| A. | 玻璃管中的固體由黑色逐漸變成紅色 | |
| B. | 剩余固體7.6g是得到的鐵的質量 | |
| C. | 生成CO2的質量為2.4 g | |
| D. | 鐵礦石樣品中Fe2O3的質量分數為80% |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 1 個 | B. | 2 個 | C. | 3 個 | D. | 4 個 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com