
某有機物在氧氣中完全燃燒,生成二氧化碳和水的質量比為22:9,則該有機物可能是( )
|
| A. | C2H4 | B. | C12H22O11 | C. | C6H12O6 | D. | C2H5OH |
| 質量守恒定律及其應用;化合物中某元素的質量計算.. | |
| 專題: | 元素質量守恒. |
| 分析: | 根據二氧化碳和水的質量比為22:9,可計算出碳、氫兩種元素的質量比為:(22×):(9×)=6:1,則碳氫的原子個數比是: =1:2. |
| 解答: | 解:根據二氧化碳和水的質量比為22:9,可計算出碳、氫兩種元素的質量比為:(22× A、C2H4中碳氫兩種原子個數比為1:2,故A正確; B、C12H22O11中碳氫兩種原子個數比為6:11,故B錯誤; C、C6H12O6碳氫兩種原子個數比為1:2,故C正確; D、C2H5OH中碳氫兩種原子個數比為1:3,故D錯誤. 故選AC. |
| 點評: | 本題主要考查有關化學式的計算,難度較小.關鍵是要學會由物質質量求原子個數比的方法. |


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:
下列圖形能正確反映對應變化關系的是( )
| A | B | C | D |
|
|
|
|
|
| 加熱一定量氯酸鉀和二氧化錳混合物 | 在密閉容器中,甲烷完全燃燒 | 碳在盛有氧氣的密閉集氣瓶內燃燒 | 電解水 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:
據中央電視臺6月3日對云南撫仙湖底古城考古的現場報道,科學家曾經通過測定古生物遺骸中的碳﹣14來推斷古城年代.碳﹣14原子的核電荷數為6,質子數和中子數之和為14,下列關于碳﹣14原子的說法中錯誤的是( )
|
| A. | 質子數為6 | B. | 中子數為6 |
|
| C. | 電子數為6 | D. | 電子數和中子數之和為14 |
查看答案和解析>>
科目:初中化學 來源: 題型:
下列事實不能說明分子之間有間隔的是( )
|
| A. | 打氣筒將空氣壓入自行車胎內 |
|
| B. | 空氣受熱體積膨脹 |
|
| C. | 氫氣在氧氣中燃燒生成水 |
|
| D. | 1體積酒精和1體積水混合小于2體積 |
查看答案和解析>>
科目:初中化學 來源: 題型:
在一定條件下,在一個密閉容器內發生某反應,測得反應過程中各物質的質量如下表所示,下列說法錯誤的是( )
| 物質 | a | b | c | d |
| 反應前質量(g) | 18 | 1 | 2 | 32 |
| 反應后質量(g) | 待測 | 26 | 2 | 12 |
|
| A. | 該反應是分解反應 |
|
| B. | d兩種物質中元素種類一定與b物質中元素種類相同 |
|
| C. | c物質可能是該反應的催化劑 |
|
| D. | 反應中a、d的質量比為1:4
|
查看答案和解析>>
科目:初中化學 來源: 題型:
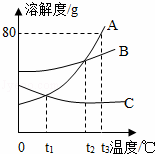
右圖為A、B、C在水中的溶解度曲線圖:
(1)A、C交點的意義是 ;
(2)t3℃時,A、B、C三者的溶解度由大到小的順序是 ;若在該溫度時將45克A放入50克水中,形成的溶液是 溶液;(填“飽和”或“不飽和”)所得溶液的質量分數為 ;
(3)如果有A、B的混合物(含少量的B),將A分離出來的方法是 ;
(4)t2℃時,等質量的A、B、C三種物質的飽和溶液,溫度升高到t3℃,所得溶液溶質質量分數由大到小的順序是: .
查看答案和解析>>
科目:初中化學 來源: 題型:
美國兩位科學家利用碘元素,借助放射學進行了“G蛋白偶聯受體”研究,揭開了“細胞如何感知周圍環境”之謎,獲得了2012年諾貝爾化學獎.圖①和圖②是碘元素在元素周期表中的部分信息及碘原子的結構示意圖.請回答:
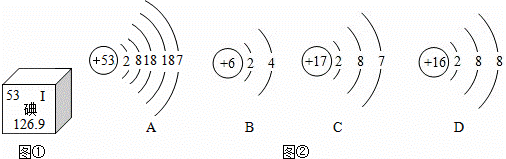
(1)由圖①可知碘元素的一點信息是: ;
(2)A、B、C中與碘元素化學性質相似的是 (填字母);
(3)碘元素在元素周期表中排在第 周期;
(4)碘化鎂的化學式是 .
查看答案和解析>>
科目:初中化學 來源: 題型:
小明同學對“鋅與硫酸反應快慢的影響因素”進行了探究。
【提出 問題】鋅與硫酸反應的快慢受哪些因素的影響呢?
問題】鋅與硫酸反應的快慢受哪些因素的影響呢?
【猜想與假設】
a.可能與硫酸的質量分數有關;
b.可能與鋅的形狀有關。
【查閱資料】
鋅的化學性質比較活潑,在常溫下的空氣中,表面生成一層“保護膜”,可阻止進一步氧化。該“保護膜”可以和酸反應,但不產生氫氣。
【設計并實驗】小兵用不同質量分數的硫酸和不同形狀的鋅進行如下實驗。
| 實驗編號 | 硫酸的質量分數(均取20mL) | 鋅的形狀(均取1g) | 氫氣的體積(mL)(均收集3分鐘) |
| ① | 20% | 鋅粒 | 31.7 |
| ② | 20% | 鋅片 | 50.9 |
| ③ | 20% | 鋅粒 | 61.7 |
| ④ | 30% | 鋅 | 79.9 |
(1)寫出稀硫酸與鋅反應的化學方程式______________________________。
(2)小兵用圖裝置收集并測量氫氣的體積,其中量筒的作用是_______________________,
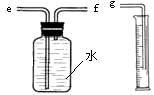 氫氣應從________(填e或f或g)管通入;
氫氣應從________(填e或f或g)管通入;
【收集證據】
(3)要比較不同質量分數的硫酸對反應快慢的影響,應選擇的實驗編號是____________;
【得出結論】
(4)結論是_____________________________________________________;
【評價與反思】
(5)下表是小兵第①組實驗的詳細數據。
| 時段(均為1分鐘) | 第1分鐘 | 第2分鐘 | 第3分鐘 | 第4分鐘 | 第5分鐘 | 第6分鐘 |
| H2的體積 | 3.1mL | 16.7mL | 11. | 9.6mL | 7.6mL | 6.0mL |
請描述鋅與硫酸反應的先慢后快最后又變慢的原因___________________________;
(6)你認為鋅與硫酸反應的快慢可能還受 因素影響?
(7)取某廠生產的生鐵樣品6g,與100g足量的稀硫酸充分反應后,稱得剩余物質的總質量為105.8g。
①生成氣體的質量為 克;
②該廠生產的生鐵樣品中鐵的質量分數是多少?(寫出具體的過程,結果精確到0.1%)
③該廠生產的生鐵是否合格? (填“合格”或“不合格”)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com