
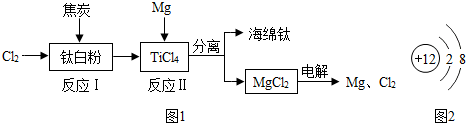
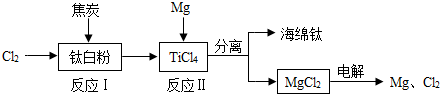
(8分)21世紀是鈦的世紀.下面是利用鈦白粉(TiO2)生產海綿鈦(Ti)的一種工藝流程:

(1)反應Ⅰ在800~900℃的條件下進行,還生成一種可燃性無色氣體,該反應的化學方程式為 _________ _;
(2)回答下列問題;
①如圖為鎂元素的某種粒子結構示意圖,該圖表示(填序號) _________ .

A.分子 B.原子 C.陽離子 D.陰離子
鎂原子在化學反應中容易失去電子,鎂是一種(填“活潑”或“不活潑”) _________ 金屬.除了能與氧氣反應,還可以與氮氣,二氧化碳等反應.
②已知氮化鎂中氮元素的化合價為﹣3價,氮化鎂的化學式為 _________ .
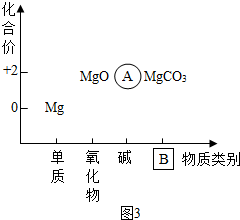
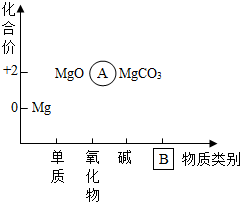
③以化合價為縱坐標,以物質的類別為橫坐標所繪制的圖象叫價類圖.如圖為鎂的價類圖,請分析該圖后填寫:

A處的化學式為: _________ , B處的物質類別是: _________ .
(3)反應II可獲得海錦鈦,化學方程式表示為TiCl4+2Mg Ti+2MgCl2.該反應在下列哪種環境中進行 _________ (填序號).
Ti+2MgCl2.該反應在下列哪種環境中進行 _________ (填序號).
A.稀有氣體中 B.空氣中 C.氮氣中 D.CO2氣體中
(4)該工藝流程中,可以循環使用的物質有 _________ .
(5)反應II可通過如下反應制得,TiCl4+2Mg Ti+2MgCl2.若要制得24g鈦,需要鎂的質量是多少克?(寫出計算過程) _________ .
Ti+2MgCl2.若要制得24g鈦,需要鎂的質量是多少克?(寫出計算過程) _________ .
(1)2Cl2+TiO2+2C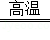 TiCl4+2CO
TiCl4+2CO
(2)①C 活潑;②Mg3N2 ③Mg(OH)2 鹽
(3)A
(4)Mg、Cl2.
(5)解:設參加反應的鎂的質量為x
TiCl4 +2Mg Ti+2MgCl2
48 48
Ti+2MgCl2
48 48
x 24g
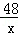 =
=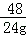 x=24g
x=24g
答:需要參加反應的鎂的質量為24g.
【解析】(1)由流程圖及題中信息可知反應物為氯氣、二氧化鈦和焦炭,生成物為四氯化鈦和一種可燃性氣體,根據反應前后元素種類不變,可知此可燃性氣體是由碳元素和氧元素組成的一氧化碳;
(2)①此微粒質子數為12,核外電子數為10,是鎂離子,屬于陽離子,鎂原子最外層上應該有2個電子,易失去電子成為陽離子,屬于活潑的金屬元素.
②根據化合物中正負化合價的代數和為0,氮元素化合價為﹣3價,鎂元素為+2價,因此氮化鎂的化學式為Mg3N2;
③堿為Mg(OH)2 碳酸鎂屬于鹽.
(3)根據第(2)小題中的信息,鎂除了能與氧氣反應,還可以與氮氣,二氧化碳等反應,因此TiCl4+2Mg Ti+2MgCl2.該反應應該在稀有氣體的環境中進行.
Ti+2MgCl2.該反應應該在稀有氣體的環境中進行.
(4)由工業流程圖可知生成物中的鎂和氯氣可循環使用
(5)根據化學方程式TiCl4+2Mg Ti+2MgCl2.中鈦的質量可求出參加反應的鎂的質量
Ti+2MgCl2.中鈦的質量可求出參加反應的鎂的質量


科目:初中化學 來源: 題型:

 圖為鎂元素的某種粒子結構示意圖,該圖表示(填序號)
圖為鎂元素的某種粒子結構示意圖,該圖表示(填序號)

| ||
| ||
| ||
查看答案和解析>>
科目:初中化學 來源: 題型:
| ||
| ||
| ||
查看答案和解析>>
科目:初中化學 來源: 題型:

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化學 來源: 題型:
| ||
| ||
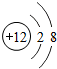
| ||
| ||
查看答案和解析>>
科目:初中化學 來源: 題型:


| ||
| ||
| ||
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com