
【題目】液氧轉化為氧氣的過程中,發(fā)生的變化是
A.混合物變?yōu)榧儍粑?/span> B.分子間的空隙增大
C.化學性質發(fā)生變化 D.分子總數(shù)增加
科目:初中化學 來源: 題型:
【題目】某校化學興趣小組的同學根據(jù)實驗室提供的儀器和藥品,在老師的指導下從下圖中選擇裝置進行了氧氣的制備實驗。

(1)寫出儀器a的名稱: 。
(2)甲同學從上圖中選擇A、E裝置的組合制取氧氣,該反應的化學方程式為: .在用膠皮管連接裝置A和E中的玻璃導管時,應先把玻璃管口 ,然后稍稍用力把玻璃管插入膠皮管。收集氣體前,應將集氣瓶裝滿 并蓋上 。收集氧氣還可選用的裝置是 。
(3)乙同學稱取一定質量的![]() 固體放入大試管中,將溫度控制在250℃加熱制取
固體放入大試管中,將溫度控制在250℃加熱制取![]() 。該反應的化學方程式為
。該反應的化學方程式為![]() 。實驗結束時,乙同學發(fā)現(xiàn)用排水法收集到的
。實驗結束時,乙同學發(fā)現(xiàn)用排水法收集到的![]() 大于理論產量。針對這一現(xiàn)象,同學們進行了如下探究:
大于理論產量。針對這一現(xiàn)象,同學們進行了如下探究:
[提出猜想]猜想I:反應生成的![]() 分解放出
分解放出![]() ;
;
猜想II:反應生成的![]() 分解放出
分解放出![]() ;
;
猜想III:反應生成的![]() 和
和![]() 分解都放出
分解都放出![]() 。
。
[實驗驗證]同學們分成兩組,分別進行下列實驗:
第一組同學取一定質量的![]() ,在250℃條件下加熱一段時間,冷卻后測得
,在250℃條件下加熱一段時間,冷卻后測得![]() 的質量不變,則猜想____錯誤;第二組同學取
的質量不變,則猜想____錯誤;第二組同學取![]() 在250℃條件下加熱,沒有用測定質量的方法得出了猜想II正確的結論。該組同學選擇簡單的實驗方法是 .
在250℃條件下加熱,沒有用測定質量的方法得出了猜想II正確的結論。該組同學選擇簡單的實驗方法是 .
[拓展延伸]實驗發(fā)現(xiàn),![]() 固體加熱制取
固體加熱制取![]() 的反應速率很慢,但如果將KMnO4固體與
的反應速率很慢,但如果將KMnO4固體與![]() 固體混合加熱,則
固體混合加熱,則![]() 的分解速率大大加快。請說明
的分解速率大大加快。請說明![]() 在
在![]() 的分解反應中是否作催化劑 (選填“是”或“否”),為什么? .
的分解反應中是否作催化劑 (選填“是”或“否”),為什么? .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列五種物質中均含有碘元素,它們按碘的化合價的順序排列:①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]() 。則根據(jù)這種排列規(guī)律,X不可能是
。則根據(jù)這種排列規(guī)律,X不可能是
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(6分)化學興趣小組的同學對“影響金屬與鹽酸反應的劇烈程度的因素”進行了探究。
【提出問題】金屬與鹽酸反應的劇烈程度受哪些因素的影響?
【做出猜想】a.可能與金屬本身的性質有關
b.可能與鹽酸的濃度有關
【設計探究】實驗所用的金屬均已用砂紙打磨。
實驗(1)為探究猜想a,小明同學分別在兩支試管中放入相同質量的鎂片和鐵片,然后分別加入相同濃度和質量的稀鹽酸,觀察到放鎂片的試管中立即產生大量氣泡,放鐵片的試管中只產生少量氣泡,寫出鎂與鹽酸反應的化學方程式 。
從實驗現(xiàn)象可以判斷:金屬活動性Mg Fe(填“>”“<”或“=”)。
得出結論: 。
實驗(2)為探究猜想b,小組同學設計如圖裝置進行實驗,
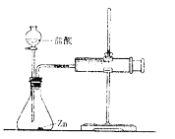
所用藥品、實驗數(shù)據(jù)如下表:
實驗編號 | 選用金屬 (均取2g) | 鹽酸濃度(均取50ml) | 每30秒產生氣體的體積/ml | |||||
30秒 | 30-60 秒 | 60-90秒 | 90-120秒 | 120-150秒 | 前150秒共收集氣體 | |||
Ⅰ | 鎂片 | 10% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
Ⅱ | 鎂片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
其中注射器的作用是 。
得出結論:金屬與鹽酸發(fā)生反應的劇烈程度與鹽酸的濃度有關,其關系是 。
【反思評價】本題獎勵4分,化學試卷總分不超過60分。
根據(jù)表中實驗Ⅱ數(shù)據(jù)分析,請描述鋅與鹽酸發(fā)生反應快慢的變化情況并解釋原因 。通過以上探究,你認為金屬與鹽酸反應的劇烈程度還可能受哪些因素影響,設計實驗驗證。 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】甲、乙兩種固體物質的溶解度曲線如圖.下列說法不正確的是
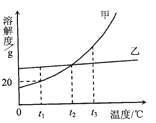
A.t2℃時,要使接近飽和的乙溶液達到飽和狀態(tài),可以用加溶質的方法
B.甲物質中含有少量乙,可采用降溫結晶的方法提純甲
C.t1℃時,50g甲的飽和溶液中溶解了10g的甲
D.將t2℃時的甲、乙兩物質的飽和溶液升溫至t3℃(溶劑的量不變),兩溶液中溶質的質量分數(shù)相等
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(4分)欲測定Cu﹣Zn合金中銅的質量分數(shù),實驗室只提供一瓶未標明質量分數(shù)的稀硫酸和必要的儀器。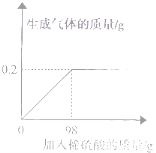 取該合金的粉末26g加入該硫酸充分反應,所加稀硫酸與生成的質量關系如圖所示。
取該合金的粉末26g加入該硫酸充分反應,所加稀硫酸與生成的質量關系如圖所示。
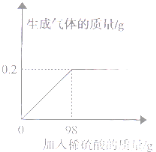
(1)生成氣體的質量為 _________ g。
(2)請計算該合金中銅的質量分數(shù).
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com