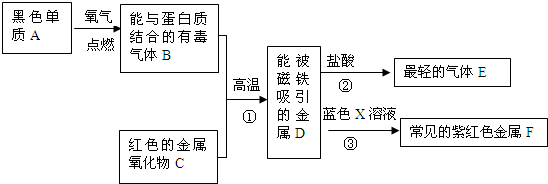
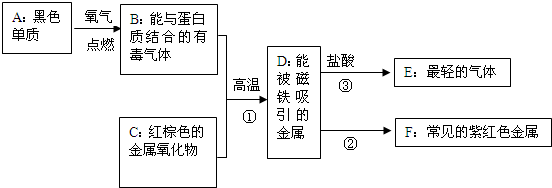
解:(1)由題給條件可知:B為一氧化碳、D是鐵、E是氫氣、F為單質銅,C物質+CO→鐵,推斷紅色金屬氧化物為氧化鐵,A+氧氣→一氧化碳,推斷A為單質碳;氫氣和一氧化碳都具還原性;工業上常用來冶煉金屬;
(2))①為一氧化碳還原氧化鐵反應方程式為:3CO+Fe
2O
3 
2Fe+3CO
2,③為鐵和硫酸銅溶液反應生成硫酸亞鐵和銅,反應的化學方程式為:Fe+CuSO
4═FeSO
4+Cu;
(3)反應③是單質和化合物反應,生成了單質和化合物為置換反應;硫酸銅溶液不能用鐵桶盛放,因為鐵能和硫酸銅溶液反應,降低藥效.
故答案為:
(1)C;CO;H
2;冶煉金屬;
(2)①3CO+Fe
2O
3 
2Fe+3CO
2;③Fe+CuSO
4═FeSO
4+Cu;
(3)置換反應;不能.
分析:本題的解題關鍵是分析反應流程:碳

CO
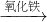
鐵

氫氣.鐵
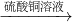
銅.
(1)首先尋找解題突破口,B是能與血紅蛋白結合的有毒氣體,則B為一氧化碳,D是能被磁鐵吸引的金屬,初中化學中常見的是金屬鐵,E是最輕的氣體,為氫氣,F是常見的紫紅色金屬,為單質銅,據此可推斷出其他物質;氫氣和一氧化碳都具還原性;
(2)①為一氧化碳還原氧化鐵,③為鐵和藍色溶液硫酸銅反應生成硫酸亞鐵和銅;
(3)反應③是單質和化合物反應,產物也是單質和化合物,符合置換反應類型;硫酸銅溶液不能用鐵桶盛放.
點評:本題屬于框圖推斷題,解此類試題首先要找題眼,即解題突破口,本題的突破口很多,如B是能與血紅蛋白結合的有毒氣體,則B為一氧化碳,D是能被磁鐵吸引的金屬,初中化學中常見的是金屬鐵,E是最輕的氣體,為氫氣,F是常見的紫紅色金屬,為單質銅,剩下的物質則很好推斷.學生在平時學習中應多注意積累常見物質的特性及用途,做推斷題才能做到得心應手.


 2Fe+3CO2,③為鐵和硫酸銅溶液反應生成硫酸亞鐵和銅,反應的化學方程式為:Fe+CuSO4═FeSO4+Cu;
2Fe+3CO2,③為鐵和硫酸銅溶液反應生成硫酸亞鐵和銅,反應的化學方程式為:Fe+CuSO4═FeSO4+Cu; 2Fe+3CO2;③Fe+CuSO4═FeSO4+Cu;
2Fe+3CO2;③Fe+CuSO4═FeSO4+Cu; CO
CO 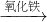 鐵
鐵  氫氣.鐵
氫氣.鐵 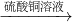 銅.
銅.