
【題目】《神秘島》是儒勒·凡爾納海洋三部曲的第三部,講述了美國南北戰爭時期,被困在南軍城中的幾個北方人乘氣球逃脫之后,飄落到“林肯島”上求生的故事。
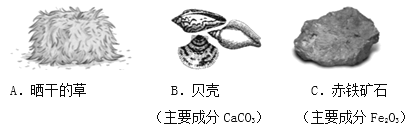
(1)將兩片懷表上的玻璃合在一起,中部灌滿水,邊緣用泥粘合,制成凸透鏡;用透鏡集聚太陽光,照射下列物質,可以燃燒起來的是_______(填字母序號,下同)。
(2)將島上的水生植物曬干、焚燒后,可獲得Na2CO3等。Na2CO3中含有_______種元素。
(3)將赤鐵礦石和木炭一層又一層疊加起來,用鼓風機吹進空氣,高溫加熱后可以獲得鐵。寫出一氧化碳與赤鐵礦石反應的化學方程式:_______。
(4)島上的黃鐵礦(主要成分為FeS2)在空氣中高溫加熱時生成一種有激性氣味的氣體,該氣體可用來制造硫酸。這種氣體是_______。
A.O2 B.Fe C.SO2 D. NH3
【答案】 A 3 Fe2O3 + 3CO![]() 2Fe + 3CO2 C
2Fe + 3CO2 C
【解析】(1)根據燃燒的條件解答;
(2)根據Na2CO3的組成分析解答;
(3)根據反應物、生成物、反應條件、質量守恒定律及化學方程式的書寫規則書寫;
(4)根據質量守恒定律分析解答。
解:(1)燃燒的條件是可燃物、空氣(或氧氣)、溫度達到可燃物的著火點。
曬干的草是可燃物,貝殼、赤鐵礦石不是可燃物。可以燃燒起來的是曬干的草。故選A;
(2)Na2CO3由鈉、碳、氧三種元素組成。故填:三。
(3)赤鐵礦石的主要成分是氧化鐵。一氧化碳與赤鐵礦石在高溫的條件下反應生成鐵和二氧化碳。反應的化學方程式:Fe2O3 + 3CO高溫2Fe + 3CO2 ;
(4)黃鐵礦(主要成分為FeS2)在空氣中高溫加熱時生成一種有激性氣味的氣體,根據質量守恒定律可知該氣體為SO2。故選C。


科目:初中化學 來源: 題型:
【題目】請沿用科學家認識事物的方式認識“水”。
①從分類角度:蒸餾水_____(填“是”或“不是”)氧化物;
②從微觀角度:構成水的微粒是______(填名稱);
③從變化角度:自來水廠凈水過程中用到活性炭,其作用是______。凈水過程中常用液氯(Cl2)作消毒劑,液氯注入水后發生反應的微觀示意圖如下:
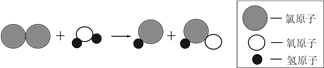
在上述反應前后,存在形態沒有發生改變的元素是_____。
④從應用角度:生理鹽水的溶劑為______;
⑤從環保角度:提倡節約用水,保護水資源。不合理的做法是______。
A.淘米水澆花
B.使用節水龍頭
C.廢水處理達標后排放
D.實驗后的廢液直接倒入下水道
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】請用下列實驗裝置完成氣體的制取及性質實驗。
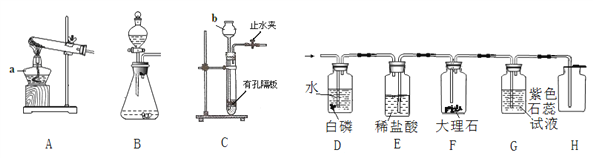
(1)儀器a的名稱________,b的名稱__________。
(2)用雙氧水和二氧化錳混合制氧氣,為了得到平穩的氧氣流,應該選擇的發生裝置是_____(填序號),反應的化學方程式為________;當產生的氧氣從D的左邊導管通入時,很快看到G中導管口有氣泡冒出。D中白磷始終沒有燃燒的原因是_________ ;E中觀察到的現象是 _________。
(3)實驗過程中,F中反應的化學方程式為________;G中溶液由紫色變紅色,G中顏色變化的原因是______(用化學方程式表示)。
(4)用H裝置可以收集剩余氣體,H裝置收集氣體的依據是_______________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列關于 C+ H2O![]() X + H2 的說法正確的是
X + H2 的說法正確的是
A. X是單質 B. 參加反應的各物質的質量比為1:1
C. X的相對分子質量為44 D. 該反應屬于置換反應
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】海水中含有NaCl、Na2CO3等物質。海水脫硫技術是用海水吸收燃煤煙氣中SO2。

(1)海水脫硫設備中,排出的海水呈堿性的是_______(填字母序號)。
A.海水泵 B.吸收塔 C. 曝氣池① D.曝氣池②
(2)向曝氣池①內通入空氣后,發生的主要化學反應如下:
i. 2H2SO3 + O2 ==== 2H2SO4
ii. 2Na2SO3 + O2 ==== 2Na2SO4
反應i、ii中化合價升高的元素是_______。
(3)曝氣池②排放的海水中不含H2SO4的原因是_______(用化學方程式解釋)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某小組同學在查閱“氫氧化鈉使酚酞變紅的原因”時,看到了以下資料。
【資料】
i.實驗室所用酚酞溶液pH < 8。溶液中,酚酞的分子結構會隨著pH的改變而改變,不同的結構在溶液中會表現出不同的顏色,具體如下表所示。
溶液的pH | 1≤pH<8 | 8≤pH≤13 | pH>13 |
酚酞的分子結構 | 內酯式 | 醌式 | 羧酸式 |
酚酞溶液的顏色 | 無色 | 紅色 | 無色 |
ii.醌式結構的酚酞能與H2O2溶液發生反應,生成無色物質,該物質在溶液中的顏色不會隨著pH的改變而改變。
iii.NaOH溶液濃度越大,溶液pH越高。
該小組同學對上述資料產生了興趣,決定對酚酞溶液顏色的變化開展探究。
【進行實驗】
組別 | 實驗操作 | 實驗現象及數據 |
1 | 1-1:配制pH為13的NaOH溶液,取5 mL于試管中,向其中滴加2滴酚酞溶液后,分成兩等份 | |
1-2:向一支試管中加入稀鹽酸 | 溶液紅色褪去 | |
1-3:向另一支試管中加入 | 溶液紅色褪去 | |
組別 | 實驗操作 | 實驗現象及數據 |
2 | 2-1:分別配制pH為8、10、11、13 的NaOH溶液,各取5 mL分別 加入4支試管中,再分別向4支 試管中加入5滴30 % H2O2溶 液,最后各滴入2滴酚酞溶液 | 每支試管中溶液都先變成紅色, 然后紅色逐漸褪去, 各支試管褪色時間如下圖所示:
|
2-2:配制pH為9的NaOH溶液,分別取5 mL加入4 支試管中,再向各試管加入5滴質量分數分別為0.5%、1%、2% 、4%的H2O2溶液, 最后各滴入2滴酚酞溶液 | 每支試管中溶液都先變成紅色, 然后紅色逐漸褪去, 各支試管褪色時間如下圖所示:
|
【解釋與結論】
(1)實驗1-1中,可以觀察到的實驗現象是_______。
(2)實驗1-2中,溶液紅色褪去的原因是_______(用化學方程式表示)。
(3)實驗1-3的目的是驗證“pH>13時,紅色酚酞溶液會變成無色”,請補全實驗操作_______。
(4)由實驗2-1可以得到結論:H2O2能使變紅的酚酞褪色,_______。
(5)實驗2-2的目的是_______。
【反思與評價】
(6)小組中某位同學在進行實驗2-1時,滴加30 % H2O2溶液,振蕩、靜置30 min后,才向溶液中加入2滴酚酞溶液。靜置過程中,他觀察到有氣泡產生;加入酚酞溶液后,他發現4支試管的褪色時間均長于原實驗2-1。導致酚酞褪色時間變長的原因可能是_______。(忽略NaOH與空氣中CO2的反應)
(7)該小組同學欲繼續探究導致紅色酚酞溶液褪色的原因。
實驗操作 | 實驗現象 |
配制pH為14的NaOH溶液,取5 mL于試管中,加入5滴30 % H2O2溶液,再滴入2滴酚酞溶液 | 溶液先變紅,后褪色 |
分析導致上述溶液先變紅后褪色的可能原因:_______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列框圖中的物質均為初中化學常見物質,其中A為大理石主要成分,F是黑色粉末,H是藍色沉淀,如圖是它們之間的轉化關系,請回答:

(1)寫出下列物質的化學式:A______D____,F____.
(2)寫出G+E→H的化學方程式:______.
(3)寫出F→B的化學反應方程式:______.
(4)寫出物質B的一種用途:______.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com