
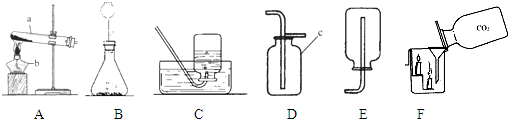
 K2MnO4+MnO2+O2↑,收集較純凈的氧氣用排水法;
K2MnO4+MnO2+O2↑,收集較純凈的氧氣用排水法; 2H2O+O2↑;二氧化錳在此反應中起催化作用;驗證氣體是否集滿可用帶火星的木條放于集氣瓶口,觀察是否復燃;
2H2O+O2↑;二氧化錳在此反應中起催化作用;驗證氣體是否集滿可用帶火星的木條放于集氣瓶口,觀察是否復燃; K2Mn04+Mn02+02↑;C;
K2Mn04+Mn02+02↑;C; 2H2O+O2↑;催化;將帶火星的木條放在瓶口,木條復燃,證明已滿;
2H2O+O2↑;催化;將帶火星的木條放在瓶口,木條復燃,證明已滿;

科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解

| ||
| ||

| 實驗 | 實驗現象 | 實驗內容 |
| A | 劇烈反應,迅速放出大量氣泡 | 反應速率過快,氣體不便收集,不宜于實驗室制取二氧化碳 |
| B | 產生氣泡,速率減慢,反應停止. | 無法持續產生CO2,不能用于實驗室制CO2 |
| C | ① 產生大量氣泡 產生大量氣泡 |
② 反應速率適中,氣體便于收集 反應速率適中,氣體便于收集 |
查看答案和解析>>
科目:初中化學 來源:2012-2013學年福建省泉州市洛江區九年級(上)期中化學試卷(解析版) 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com