
| 3.5g |
| 10g |
| 65 |
| 6.5g |
| 98 |
| x |
| 9.8g |
| 49.0 |


科目:初中化學 來源: 題型:閱讀理解

| 猜想 | 簡單實驗方案 | 現象 | CO和CuO反應的化學方程式 |
| 粉末為Cu | 不反應 | CuO+CO=Cu+CO2 | |
| 粉末溶解,溶液變成藍色,生成紅色粉末 | 2CuO+CO=Cu2O+CO2 |

查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
 金屬與人類的生活和生產密切相關.
金屬與人類的生活和生產密切相關.| 實驗步驟 | 現象和結論 | 有關反應的化學方程式 |
| 取少量濾紙上剩余的物質置于試管中,向其中滴加適量的 |
||
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
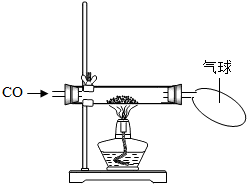
| 猜想 | 簡單實驗方案 | 現象 | CO和CuO反應的化學方程式 |
| 粉末為Cu | 不反應 | CuO+CO=Cu+CO2 | |
| 粉末溶解,溶液變成藍色,生成紅色粉末 | 2CuO+CO=Cu2O+CO2 |
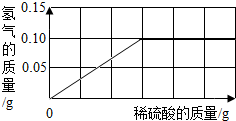
查看答案和解析>>
科目:初中化學 來源:2009-2010學年江蘇省鎮江市鎮江四中九年級(上)期末化學試卷(解析版) 題型:解答題

| 猜想 | 簡單實驗方案 | 現象 | CO和CuO反應的化學方程式 |
| 粉末為Cu | 不反應 | CuO+CO=Cu+CO2 | |
| 粉末溶解,溶液變成藍色,生成紅色粉末 | 2CuO+CO=Cu2O+CO2 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com