
 日常生活中接觸的金屬材料,大多屬于合金.其中黃銅是以鋅作主要添加元素的銅合金.已知組成某彈殼的黃銅中只含有鋅和銅,現將22g該彈殼碾成粉末后放入盛有足量的稀硫酸燒杯中,測得反應過程中生成的氫氣的質量(單位為g)與反應時間(單位為min)的關系如圖所示.試計算:
日常生活中接觸的金屬材料,大多屬于合金.其中黃銅是以鋅作主要添加元素的銅合金.已知組成某彈殼的黃銅中只含有鋅和銅,現將22g該彈殼碾成粉末后放入盛有足量的稀硫酸燒杯中,測得反應過程中生成的氫氣的質量(單位為g)與反應時間(單位為min)的關系如圖所示.試計算:分析 (1)將彈殼碾成粉末可以增大反應物的接觸面積,增大反應速率;
(2)根據圖中的信息可知氫氣的質量;
(3)銅與稀硫酸不反應.利用鋅與硫酸反應的化學方程式,根據氫氣的質量求出鋅的質量,進而求出黃銅中銅的質量;
(4)根據溶質的質量分數計算公式分析回答.
解答 解:(1)將彈殼碾成粉末可以增大反應物的接觸面積,增大反應速率;
(2)根據題意可知,生成氫氣的質量為0.2g;
(3)設黃銅中鋅的質量為x
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
$\frac{65}{2}=\frac{x}{0.2g}$
x=6.5g
彈殼中銅的質量為:22g-6.5g=15.5g;
(4)若要計算反應后所得溶液中ZnSO4的質量分數,根據鋅與硫酸反應的方程式可計算出硫酸鋅的質量,還應知道溶液的質量,所以,至少還應該補充的一個條件是稀硫酸的質量.
故答案為:
(1)大反應物的接觸面積,增大反應速率;
(2)0.2g;
(3)原樣品中銅的質量為15.5g;
(4)稀硫酸的質量.
點評 本題考查根據化學方程式的簡單計算,已知生成物的質量求反應物的質量,解題的關鍵是正確的對圖象意義的分析;


科目:初中化學 來源: 題型:解答題
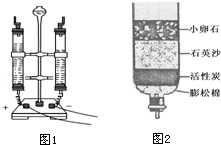 水是生命之源.
水是生命之源.查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題

查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 氧化反應都是化合反應 | |
| B. | 有氧氣參加的化學反應,一定是化合反應 | |
| C. | 化合反應只生成一種物質 | |
| D. | 氧化反應的生成物一定有兩種 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com