
| 錐形瓶 | 錐形瓶+稀鹽酸 | 錐形瓶+反應后溶液 | |
| 質量(克) | 35.5 | 55.5 | 80.5 |
分析 (1)根據溶質質量=溶液質量×溶質質量分數解答;
(2)根據質量守恒定律反應所消耗的氫氧化鈉溶液的質量=反應后所得物質的總質量-反應前所有物質的總質量;
(3)根據化學方程式結合氫氧化鈉的質量可以計算出硫酸的質量進而就算出其溶質的質量分數;
(4)根據pH值可知其用氫氧化鈉溶液過量,故計算出的結果要偏大.
解答 解:(1)需要氫氧化鈉固體的質量為:500g×16%=80g;
(2)反應所消耗的氫氧化鈉溶液質量:80.5g-55.5g=25g;
(3)設稀鹽酸的溶質質量為x,氫氧化鈉的質量=25g×16%=4g
NaOH+HCl=NaCl+2H2O
40 36.5
4g x
$\frac{40}{4g}=\frac{36.5}{x}$
解得:x=3.65g
該瓶稀鹽酸的溶質質量分數=$\frac{3.65g}{55.5g-35.5g}×$100%=18.25%
(8)根據pH值可知其用氫氧化鈉溶液過量,故計算出的結果要偏大;由于石蕊試液的變色不明顯,可以將石蕊試液換成酚酞試液.
答案:
(1)80;(2)25;(3)該瓶稀鹽酸的溶質質量分數為18.25%;(4)偏大;①取一潔凈的錐形瓶稱量,然后往其中加入一定量的稀鹽酸,并滴入幾滴酚酞試液(質量忽略不計),重新稱量;②往上述錐形瓶中逐滴加入溶質質量分數為16%的氫氧化鈉溶液,邊滴加邊振蕩,當觀察到溶液由無色恰好變為紅色時,停止滴加,再次稱量.
點評 本題主要考查學生運用化學方程式和溶質質量分數公式綜合分析和解決實際問題的能力.增加了學生分析問題的思維跨度,強調了學生整合知識的能力.解題的關鍵是分析反應物與生成物之間的質量關系.


科目:初中化學 來源: 題型:選擇題
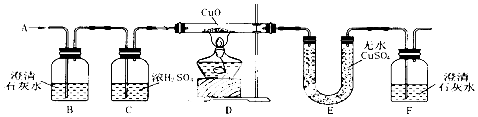
| A. | HCl、CO2、CO、H2 | B. | N2、CO2、CO、H2 | C. | HCl、CO2、CO、O2 | D. | CO2、N2、CO、O2 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
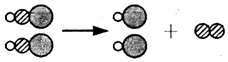
| A. | H2CO3 $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+H2O | B. | 2H2SO3+O2═2H2SO4 | ||
| C. | 2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑ | D. | CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaO+CO2↑ |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
 某研究小組在驗證“堿使酚酞試液變紅”的實驗時,發現一個意外現象:將酚酞試液滴入某NaOH溶液中,溶液變成了紅色,可是過一會兒紅色卻消失了,且不同組實驗時紅色消失的時間也不同.是什么原因導致滴有酚酞的NaOH溶液由紅色褪為無色?
某研究小組在驗證“堿使酚酞試液變紅”的實驗時,發現一個意外現象:將酚酞試液滴入某NaOH溶液中,溶液變成了紅色,可是過一會兒紅色卻消失了,且不同組實驗時紅色消失的時間也不同.是什么原因導致滴有酚酞的NaOH溶液由紅色褪為無色?查看答案和解析>>
科目:初中化學 來源: 題型:填空題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源:【全國市級聯考】重慶市2017屆九年級中考模擬(B)化學試卷 題型:選擇填充題
如圖為汽車尾氣凈化裝置中發生反應的微觀示意圖。有關敘述錯誤的是( )
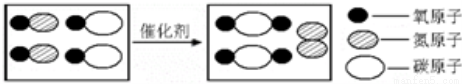
A. 圖中單質的化學式為N2 B. 該反應是化合反應
C. 反應后分子總數減少 D. 該裝置可凈化汽車尾氣
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com