
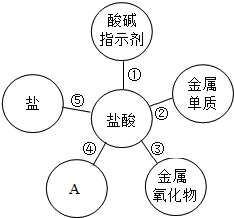
 歸納是重要的學習方法,小紅在復習鹽酸的性質是,歸納出鹽酸的五條化學性質(如圖所示,連線表示相互反應).
歸納是重要的學習方法,小紅在復習鹽酸的性質是,歸納出鹽酸的五條化學性質(如圖所示,連線表示相互反應).分析 (1)利用石蕊遇酸的變色情況分析即可.
(2)根據酸的化學性質:能與活潑金屬、金屬氧化物、酸堿指示劑、鹽、堿等反應,進行分析解答.
(3)鐵銹的主要成分是氧化鐵,與鹽酸反應生成氯化鐵和水,寫出反應的化學方程式即可.
(4)根據鹽與鹽酸反應的條件進行分析判斷.
(5)控制變量法要創設相同的外部條件,分析對鎂和鋅與鹽酸反應的快慢可能有影響的因素.
(6)①欲求被電解的水的質量,須根據電解水的化學方程式,列出比例式,即可得出;
②欲求電解后的硫酸溶液的溶質質量分數,須知反應過程中電解水的質量,原硫酸溶液質量-電解水的質量=電解后的硫酸溶液的質量,再根據溶質質量分數=$\frac{溶質質量}{溶液質量}$×100%計算即可.
解答 解:(1)石蕊遇酸性溶液會變紅色,所以將紫色石蕊試液滴加到鹽酸溶液中溶液變紅.
(2)鹽酸除了能與酸堿指示劑、金屬氧化物、金屬、鹽反應外,還能與堿發生中和反應,故A的類別是堿.
(3)鐵銹的主要成分是氧化鐵,與鹽酸反應生成氯化鐵和水,反應的化學方程式是:Fe2O3+6HCl═2FeCl3+3H2O.
(4)酸與鹽的反應一定要符合復分解反應的發生條件,所以選擇的鹽與鹽酸反應時一定會有水、氣體或沉淀生成.所以該鹽可以是硝酸銀;
(5)控制變量法要創設相同的外部條件,探究鎂和鋅與鹽酸反應的快慢,需要控制不變的條件就是對反應速度可能有影響的因素,分析可知四個因素中只有容器的大小對反應速度無影響.
(6)解:①設被電解的水的質量為x
2H2O$\frac{\underline{\;通電\;}}{\;}$2H2↑+O2↑
36 4
x lg
$\frac{36}{4}=\frac{x}{1g}$
解之得:x=9g
(2)電解后硫酸溶液的溶質質量分數為:$\frac{45g×8%}{45g-9g}$×100%=10%
答:被電解的水的質量是9g,電解后硫酸溶液的溶質質量分數是l0%.
故答案為:
(1)紅(2)堿(3)6HCl+Fe2O3═2FeCl3+3H2O;
(4)硝酸銀;(5)ABD;(6)9g;l0%
點評 本題難度不大,熟練掌握酸的化學性質、化學方程式的書寫等并能靈活運用是正確解答本題的關鍵.


 名師點睛字詞句段篇系列答案
名師點睛字詞句段篇系列答案科目:初中化學 來源: 題型:選擇題
| A. | 露天焚燒秸稈 | B. | 利用太陽能發電 | C. | 汽車排放尾氣 | D. | 直接用煤作燃料 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | CH4+2O2 $\frac{\underline{\;點燃\;}}{\;}$ CO2+2H2O | B. | CO2+Ca(OH)2═CaCO3↓+H2O | ||
| C. | CaCO3+2HCl═CaCl2+CO2↑+H2O | D. | 3CO+Fe2O3 $\frac{\underline{\;高溫\;}}{\;}$ 2Fe+3CO2 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 只含碳一種元素 | B. | 只含氫一種元素 | ||
| C. | 一定含碳和氫兩種元素 | D. | 可能含碳、氫、氧三種元素 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | ①②④ | B. | ①③⑤ | C. | ①③⑥ | D. | ②③⑥ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com