


科目:初中化學 來源: 題型:

查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解

| 實驗操作 | 實驗現象 | 實驗結論及解釋 |
| ① 取少量濾液C于試管中,加入足量CaCl2溶液 |
有白色沉淀生成 |
猜想③正確 |
| ② 過濾,在濾液中滴加無色酚酞試液 |
溶液由無色變成紅色 |
查看答案和解析>>
科目:初中化學 來源: 題型:

查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
| [小資料] ①堿石灰是氧化鈣、氫氧化鈣的固體混合物.易吸收空氣中的水蒸氣和二氧化碳. ②氯化鈣溶液顯中性.[提出問題]實驗室中久置的堿石灰樣品的成分是什么? [進行猜想]久置的堿石灰樣品中可能含有CaO、NaOH、Na2CO3、Ca(OH)2、CaCO3等成分.用化學方程式表示樣品中含有Ca(OH)2或Na2CO3可能含有的原因 CaO+H2O═Ca(OH)2(或2NaOH+CO2═Na2CO3+H2O等,答案合理即可) CaO+H2O═Ca(OH)2(或2NaOH+CO2═Na2CO3+H2O等,答案合理即可) (寫一個).[探究過程]  試回答下列問題: (1)操作①的名稱是 過濾 過濾 ,溶液C中一定含OH- OH- 離子.(2)溶液A中加入CaCl2溶液后產生固體,說明樣品中一定含有 碳酸鈉 碳酸鈉 ,反應的方程式為Na2CO3+CaCl2═2NaCl+CaCO3↓ Na2CO3+CaCl2═2NaCl+CaCO3↓ .(3)向溶液A中加入CaCl2溶液后,證明CaCl2溶液過量的方法是 取溶液C于試管中滴加碳酸鈉溶液,有白色沉淀生成,說明CaCl2溶液已過量 取溶液C于試管中滴加碳酸鈉溶液,有白色沉淀生成,說明CaCl2溶液已過量 .[實驗結論] 依據上述實驗操作過程及現象,綜合對濾液和固體成分的探究,下列對樣品成分的分析正確的是 ②③ ②③ (填序號).①樣品中一定含NaOH ②樣品中一定含Na2CO3 ③樣品中含NaOH、CaO中的一種或兩種 [拓展延伸] 為測定實驗室中一瓶變質的燒堿中NaOH的含量,某同學取適量的燒堿樣品,溶于一定量的水得到200g溶液;再加入200g稀硫酸(足量)充分攪拌到不再放出氣泡為止,稱量溶液為395.6g.請分析計算: (1)反應產生的CO2的質量為 4.4 4.4 g.(2)若所取燒堿樣品為50.0g,則樣品中NaOH的質量分數是多少?(寫出計算過程) 78.8%. 78.8%. .(3)用同濃度的硫酸,分別與未變質、部分變質、或全部變質(雜質都是Na2CO3)的燒堿樣品反應,需要硫酸的質量都相等.從鈉元素質量守恒的角度解釋其原因是: 氫氧化鈉和碳酸鈉都是每46g鈉元素生成142g硫酸鈉,消耗98g硫酸 氫氧化鈉和碳酸鈉都是每46g鈉元素生成142g硫酸鈉,消耗98g硫酸 .
查看答案和解析>> 科目:初中化學 來源: 題型:  堿石灰是實驗室常用的干燥劑.同學們為確認一瓶久置的“堿石灰”(可能已部分變質或全部變質)樣品的成分,進行如下探究. 堿石灰是實驗室常用的干燥劑.同學們為確認一瓶久置的“堿石灰”(可能已部分變質或全部變質)樣品的成分,進行如下探究. 【提出問題】實驗室中久置的堿石灰樣品的成分是什么? 【進行猜想】 久置的堿石灰樣品中可能含有CaO、NaOH、Na2CO3、Ca(OH)2、CaCO3等成分.用化學方程式表示樣品中含有Ca(OH)2或Na2CO3可能含有的原因 【探究過程】 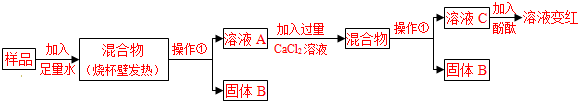 試回答下列問題: (1)操作①的名稱是 (2)溶液A中加入CaCl2溶液后產生固體,該反應的方程式為 (3)向溶液A中加入CaCl2溶液后,證明CaCl2溶液過量的方法是 【實驗結論】 依據上述實驗操作過程及現象,綜合對濾液和固體成分的探究,下列對樣品成分的分析正確的是 ①樣品中一定含NaOH ②樣品中一定含Na2CO3 ③樣品中含NaOH、CaO中的一種或兩種 【拓展延伸】 (1)為測定實驗室中一瓶變質的燒堿中NaOH的含量,某同學取50.0g燒堿樣品,溶于一定量的水中得到200g溶液;再加入200g稀硫酸(足量)充分攪拌到不再放出氣泡為止,稱量溶液為395.6g.請分析計算樣品中NaOH的質量分數是多少?(寫出計算過程) (2)用同濃度的硫酸,分別與未變質、部分變質、或全部變質(雜質都是Na2CO3)的燒堿樣品反應,需要硫酸的質量都相等.從鈉元素質量守恒的角度解釋其原因是: 查看答案和解析>> 同步練習冊答案 湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區 違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com版權聲明:本站所有文章,圖片來源于網絡,著作權及版權歸原作者所有,轉載無意侵犯版權,如有侵權,請作者速來函告知,我們將盡快處理,聯系qq:3310059649。 ICP備案序號: 滬ICP備07509807號-10 鄂公網安備42018502000812號 |