

分析 (1)試管是常用的反應容器;
(2)實驗室制取二氧化碳,為固液常溫型,利用CaCO3+2HCl═CaCl2+CO2↑+H2O來制取二氧化碳;并根據化學方程式進行計算;稀釋溶液時,溶質的質量不變;
(3)過氧化氫溶液和二氧化錳混合制取氧氣,過氧化氫分解生成水和氧氣.
解答 解:(1)試管是常用的反應容器,故答案為:試管;
(2)實驗室制取二氧化碳,為固液常溫型,組裝發生裝置可選擇如圖中的B、F、和C;
①該反應的化學方程式為:CaCO3+2HCl═CaCl2+CO2↑+H2O;
②設參加反應的CaCO3的質量為x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 2.2g
$\frac{100}{44}=\frac{x}{2.2g}$
x=5g;
③需要36%的濃鹽酸的質量為:$\frac{200g×18%}{36%}$=100g;
(3)過氧化氫分解生成水和氧氣,化學方程式為:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
故答案為:(1)試管;
(2)C;
①CaCO3+2HCl═CaCl2+CO2↑+H2O;
②5;
③100;
(3)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
點評 本考點主要考查了儀器的名稱、氣體的制取裝置和收集裝置的選擇,同時也考查了化學方程式的書寫等,綜合性比較強.


 名校課堂系列答案
名校課堂系列答案科目:初中化學 來源: 題型:推斷題
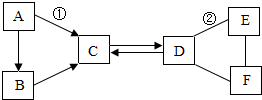 A~F是初中化學常見的六種物質,其中B、C組成元素相同,C、D、E、F是不同類別的化合物,D和E溶液均呈堿性,且E可用作建筑材料,它們相互間的關系如圖所示,(圖中“-”表示相連的物質兩兩之間可以發生反應,“→”表示由某一物質轉化為另一物質,部分反應物、生成物及反應條件已略去)請回答:
A~F是初中化學常見的六種物質,其中B、C組成元素相同,C、D、E、F是不同類別的化合物,D和E溶液均呈堿性,且E可用作建筑材料,它們相互間的關系如圖所示,(圖中“-”表示相連的物質兩兩之間可以發生反應,“→”表示由某一物質轉化為另一物質,部分反應物、生成物及反應條件已略去)請回答:查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
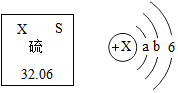 在元素周期表中,硫元素的信息如圖所示,下列從圖中獲得的信息不正確的是( )
在元素周期表中,硫元素的信息如圖所示,下列從圖中獲得的信息不正確的是( )| A. | 在硫原子的核外電子排布中 a=2 和 b=8 | |
| B. | 硫原子在化學反應中易獲得 2 個電子生成 S2- | |
| C. | 硫原子里,質子數=中子數=電子數=16 | |
| D. | 一個硫原子的相對原子質量是 32.06 克 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
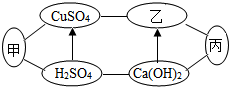 如圖中甲、乙、丙是初中化學中常見的物質,圖中“-”表示相連的物質之間可以在溶液中發生化學反應,“→”表示由某種物質可轉化為另一種物質(部分反應物、生成物及反應條件已略去).下列說法中不正確的是( )
如圖中甲、乙、丙是初中化學中常見的物質,圖中“-”表示相連的物質之間可以在溶液中發生化學反應,“→”表示由某種物質可轉化為另一種物質(部分反應物、生成物及反應條件已略去).下列說法中不正確的是( )| A. | 甲、乙、丙可能依次為Fe、NaOH、CO2 | |
| B. | 當乙為NaOH時,它由Ca(OH)2與Na2CO3反應生成 | |
| C. | 甲物質只能是堿或鹽 | |
| D. | 當甲為一種堿時,它與硫酸銅溶液的反應可能產生兩種沉淀 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:多選題
| A. | FeCl3、NaOH、HCl、KCl | B. | HCl、KNO3、Na2CO3、Na2SO4 | ||
| C. | AgNO3、HCl、NaCl、HNO3 | D. | BaCl2、Na2SO4、Na2CO3、HCl |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com