
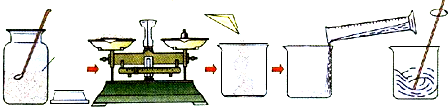
分析 (1)根據配制溶質質量分數一定的溶液的步驟分析解答需要的儀器.
(2)①利用溶質質量=溶液質量×溶質的質量分數,可根據溶液的質量和溶質的質量分數計算配制溶液所需要的溶質的質量;再根據溶劑質量=溶液質量-溶質質量即可求得水的質量.
②根據配制溶質質量分數一定的溶液的步驟,使用托盤天平稱量藥品時應遵循“左物右碼”,稱量時天平指針偏左,說明藥品質量大于砝碼質量,量筒讀數時視線要與凹液面的最低處保持水平,進行分析解答.
③根據配制溶質質量分數一定的溶液的步驟,結合硝酸鉀沒有全部溶解,會造成溶質的質量偏小,進行分析解答.
④根據配制溶質質量分數一定的溶液的步驟,進行分析解答.
解答 解:(1)配制100g溶質質量分數是1.4%的硝酸鉀溶液,首先計算配制溶液所需硝酸鉀和水的質量,再稱量所需的硝酸鉀和量取水,最后進行溶解;在這些操作中需要的儀器:托盤天平、藥匙、量筒、膠頭滴管、燒杯和玻璃棒.
(2)①溶質質量=溶液質量×溶質的質量分數,配制100g溶質質量分數是1.4%的硝酸鉀溶液,需硝酸鉀的質量=100g×1.4%=1.4g;溶劑質量=溶液質量-溶質質量,則所需水的質量=100g-1.4g=98.6g(98.6).
②配制100g溶質質量分數是1.4%的硝酸鉀溶液,首先計算配制溶液所需硝酸鉀和水的質量,再稱量所需的硝酸鉀和量取水,最后進行溶解、裝瓶貼簽;
使用托盤天平稱量藥品時應遵循“左物右碼”,稱量時天平指針偏左,說明藥品質量大于砝碼質量,應該進行的操作是減少硝酸鉀.稱量時先把砝碼放在左盤的紙上,移動游碼至總質量剛好是所需要質量.
量取水讀數時視線要與液體的凹液面的最低處保持水平.
③配制100g溶質質量分數是1.4%的硝酸鉀溶液,首先計算配制溶液所需硝酸鉀和水的質量,再稱量所需的硝酸鉀和量取水,最后進行溶解;若硝酸鉀沒有全部溶解,則溶質的質量偏小,故此時溶液的溶質質量分數要小于1.4%.
④裝瓶:把得到的溶液倒入試劑瓶,貼上標簽,放到指定位置.
故答案為:(1)量筒、膠頭滴管、玻璃棒;(2)①1.4g;98.6mL;②稱量;減少硝酸鉀;左;液體的凹液面的最低處;③溶解;小于;④標簽.
點評 本題難度不大,掌握配制溶質質量分數一定的溶液的基本步驟、注意事項、量筒的使用方法等是正確解答本題的關鍵.


 期末100分闖關海淀考王系列答案
期末100分闖關海淀考王系列答案 小學能力測試卷系列答案
小學能力測試卷系列答案科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 圖是某天然礦泉水的商標,據此請把帶括號的部分用恰當的化學用語填空:
圖是某天然礦泉水的商標,據此請把帶括號的部分用恰當的化學用語填空:查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com