
【題目】某粗鹽中除NaCl以外還含有少量雜質MgCl2,為了測定粗鹽中MgCl2的質量分數,取固體樣品25.0g完全溶解于75.0g水中,并向其中逐漸加入一定濃度的NaOH溶液,實驗過程中生成沉淀的質量與加入NaOH溶液的質量的關系如圖所示:
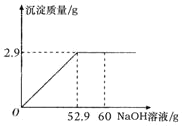
請根據相關信息完成下列計算:
(1)粗鹽樣品中氯化鎂的質量分數。
(2)恰好完全反應時得到的溶液中溶質的質量分數。
 字詞句篇與同步作文達標系列答案
字詞句篇與同步作文達標系列答案科目:初中化學 來源: 題型:
【題目】化學興趣小組用如圖裝置進行實驗,發現鎂片完全溶解、石灰水渾濁。
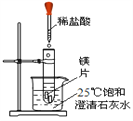
(一)石灰水變渾濁的原因是:
(1)鎂和鹽酸的反應________(填“吸熱”或“放熱”)。
(2)_____________________________________________。
(二)甲同學測得反應后試管內溶液pH<7 ,該溶液pH<7的可能原因是:
①MgCl2溶液的pH<7; ②__________________________。
(三)乙同學將反應后試管內溶液冷卻,加入鎂粉并滴入酚酞,溶液顏色無變化,再加熱,發現溶液慢慢渾濁且變紅。
【猜想】對實驗中“溶液慢慢渾濁且變紅”的原因,乙同學提出猜想:
MgCl2+2H2O=Mg(OH)2↓+2HCl,大家都認為此猜想不合理,理由是_________。
【查閱】資料1:Mg(OH)2難溶解于水,升高溫度可加大其在水中的溶解度。
資料2:K、Ca、Na、Mg等活潑金屬在一定條件下能與水反應,產生堿和氣體。
【實驗】乙同學重新在滴有酚酞的熱水中加入鎂粉,觀察到液體慢慢變紅并渾濁,鎂粉表面產生氣泡。收集并點燃氣體,發現能燃燒。乙同學實驗中“溶液慢慢渾濁且變紅”的原因請用化學方程式表示:___________________。
(四)丙同學在做實驗時,不小心將鎂條掉入到碳酸氫鈉溶液中,發現產生大量的氣泡和白色不溶物。他非常好奇,進行了如下探究。
【提出問題】鎂條與碳酸氫鈉溶液反應,產生的氣體和白色不溶物分別是什么?
【查閱資料】
Mg(OH)2 | MgCO3 | |
溶解性 | 難溶于水 | 微溶于水 |
熱穩定性 | 受熱易分解,能生成兩種氧化物 | 受熱易分解,能生成兩種氧化物 |
實驗探究一:鎂條與碳酸氫鈉溶液反應產生什么氣體呢?
猜想 | 實驗方法 | 現象 | 結論 | |
① | 二氧化碳 | 收集氣體于集氣瓶中,而后將氣體通入澄清石灰水中; | 無明顯現象 | 猜想①不成立 |
② | 氧氣 | 收集氣體于集氣瓶中,而后將________放入瓶中; | 無明顯現象 | 猜想②不成立 |
③ | 氫氣 | 第一步,點燃產生的氣體; 第二步,在火焰上罩內壁涂有石灰水的燒杯。 | 氣體能被點燃; 燒杯內壁無現象; | 猜想______成立 (填序號) |
④ | _____ | |||
⑤ | 甲烷 | |||
實驗探究二:
【提出問題】鎂條與碳酸氫鈉溶液反應,產生的白色不溶物是什么?
【作出猜想】丙同學根據資料分析認為白色不溶物可能是Mg(OH)2和MgCO3中的一種或兩種。
【進行實驗】
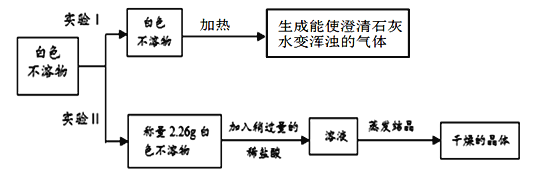
(1)根據實驗Ⅰ的現象,寫出加熱白色不溶物時一定發生的化學反應的方程式__________;
(2)實驗Ⅱ中 稱量“干燥的晶體”質量為2.85g,由此通過計算確定白色不溶物是成分是_________________。(請你寫出計算過程)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】根據下列裝置圖,回答有關問題:
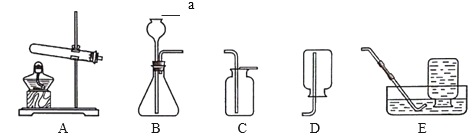
(1)寫出裝置圖中標號儀器的名稱:a____。
(2)實驗室用高錳酸鉀制取氧氣,其發生裝置可選擇____(填字母),反應的化學方程式是____。可用E裝置收集氧氣的原因是____。
(3)實驗室通常用裝置B與____(填字母)相連制取二氧化碳,該反應化學方程式是____。用右圖所示裝置制二氧化碳,有“隨開隨用、隨關隨停”的效果。在反應的過程中,若關閉導管上的活塞K,反應停止,其原理是____。
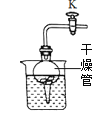
(4)用純凈的二氧化碳氣體按右圖裝置進行實驗。觀察到的主要現象是:甲中____、乙中澄清石灰水變渾濁。乙中發生反應的化學方程式為____。
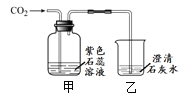
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】X、Y 兩種固體物質的溶解度曲線如右圖所示。下列說法正確的是
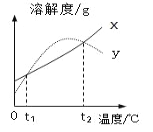
A. t1℃時 X 的飽和溶液升溫至 t2℃時仍是飽和溶液
B. 分別將 t1℃時 X、Y 的飽和溶液升溫至 t2℃,所得溶液中溶 質的質量分數相等
C. 相同溫度時,X 的溶解度一定大于 Y 的溶解度
D. Y 的溶解度隨溫度的升高而增大
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗室利用某過氧化氫溶液制取氧氣,向100g 過氧化氫溶液中加入5g 的二氧化錳,充分反應后,過濾,得到濾液97.2g,則原過氧化氫溶液中氫元素的質量分數是( )
A. 10.8%B. 35%C. 0.35%D. 5.9%
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】向兩支試管中分別加入2毫升蒸餾水,然后各滴入1到2 滴石蕊溶液,觀察試管中溶液的顏色。將其中一支試管靜置。向另一支試管中通入二氧化碳,觀察現象,并與靜置的試管中溶液的顏色進行對比。將通入二氧化碳的試管放在酒精燈火焰上加熱,觀察現象。
(1)證明水不能使石蕊溶液變色的實驗操作及現象是_________。
(2)該實驗證明二氧化碳和水反應生成了______,能使石蕊溶液變_____。
(3)加熱涉及的反應化學方程式為_________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】金屬材料同人類文明的發展和社會的進步關系十分密切。
(一)鐵的廣泛應用
(1)人體缺鐵會造成貧血,這里的鐵是指_________。(選填序號)
A.單質 B.元素 C.原子
(2)雙吸劑的主要成分是鐵粉,作用是防潮和防氧化,原理是鐵銹蝕,過程中吸收_______。
(3)暖寶寶的主要成分是鐵粉、氯化鈉等,原理也是鐵銹蝕,銹蝕過程中發生__________。
A.劇烈氧化 B.緩慢氧化
(二)鐵的冶煉
實驗室用工業鐵紅(主要成分是Fe2O3,還含有少量的FeO、Fe3O4)模擬工業煉鐵并測定鐵紅中鐵元素的質量分數,進行了實驗,裝置如下:
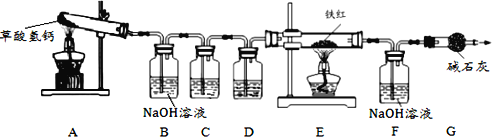
【資料】1.草酸氫鈣是白色固體,化學式為Ca(HC2O4)2,加熱易分解,生成四種氧化物
2.NaOH溶液能很好地吸收CO2,堿石灰能吸收CO2和H2O。
3.濃硫酸具有吸水性,是氣體干燥劑。
【問題討論】
(1)實驗前應先________________。
(2)寫出A中發生的反應化學方程式___________________。
(3)進入E中的氣體是純凈、干燥的CO,則C、D中的試劑依次是_______、_______(選填序號)。
a.濃硫酸 b.澄清的石灰水 c. 氫氧化鈉溶液
(4)C裝置的作用是_________________。
(5)實驗結束后,對E裝置停止加熱,繼續通入CO至冷卻,其目的是:______________。
(6)寫出E裝置中Fe2O3所發生的反應化學方程式________________。
(7)稱取鐵紅樣品7.0 g,用上述裝置進行實驗,測定鐵紅中鐵元素的質量分數。
實驗前后稱得F裝置增重4.4g,則此鐵紅中鐵元素的質量分數是____________。
【實驗反思】
1.本實驗中如果缺少G裝置(不考慮其它因素),則測得樣品中鐵的質量分數會_________(填“偏大”、“不變”或“偏小”)。
2.請指出上述實驗裝置的一個明顯缺陷_________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗室有一包含雜質的碳酸氫鈉樣品100g(雜質不含鈉元素,受熱不變化),其中鈉元素質量分數為23%,180℃時,將樣品加熱一段時間后稱得固體質量為87.6g,則分解的碳酸氫鈉占原碳酸氫鈉的質量分數為(2NaHCO3![]() Na2CO3 + H2O + CO2↑)
Na2CO3 + H2O + CO2↑)
A. 33.6% B. 40% C. 47.3% D. 60%
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com