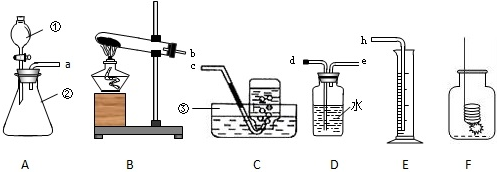
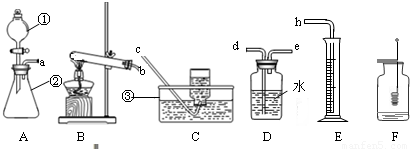
解:(1)熟悉常見儀器的名稱和用途,圖中①是分液漏斗,②錐形瓶,③是水槽;
(2)反應物的狀態是固體和液體,需要加熱,所以我們可以選用裝置B作為發生裝置;根據反應物是高錳酸鉀,反應條件是加熱,生成物是錳酸鉀、水、氧氣寫出化學反應式配平即可.
(3)測氣體體積要根據氣體排出水的體積來看氣體體積.為達到實驗目的,粗略測定加熱一定質量的高錳酸鉀所收集到的氧氣體積,可測定排出水的體積,因此各裝置的正確連接順序是b→d→e;原試管中存在的氧氣或錳酸鉀繼續分解出氧氣導致收集到的氧氣的體積比計算出的理論值偏大.故答案為:b→d→e、原試管中的空氣中的氧氣或錳酸鉀繼續分解出氧氣;
(4)沒有觀察到“劇烈燃燒、火星四射”的實驗現象可能是沒有收集到純凈的氧氣,或鐵絲有銹,沒有達到著火點等.
(5)過氧化氫和二氧化錳來制取氧氣的發生裝置是A,化學方程式為2H
2O
2
2H
2O+O
2↑.
故答案為:(1)分液漏斗,錐形瓶,水槽;
(2)B,2KMnO
4
K
2MnO
4+MnO
2+O
2↑;
(3)BDE
(4)瓶內氧氣不純或鐵絲表面的銹未除去等.
(5)A,2H
2O
2
2H
2O+O
2↑.
分析:(1)熟悉常見儀器,了解名稱;
(2)用高錳酸鉀制取氧氣,需要加熱反應;根據反應物、反應條件、生成物寫出化學反應式;
(3)根據氣體排出水的體積測出氣體體積,據此連接實驗裝置;偏大可能是因為試管中原有的氧氣等原因造成的;
(4)根據實驗可能造成失敗的原因來考慮,如氧氣不純、鐵絲表面生銹.
(5)過氧化氫是液體,二氧化錳是固體,選擇發生裝置根據這些.
點評:本題考查實驗儀器的作用、反應式的書寫、實驗儀器的選擇,需要同學們了解反應物的狀態、反應條件、生成物的性質與實驗裝置之間的關系.


 2H2O+O2↑.
2H2O+O2↑. K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑; 2H2O+O2↑.
2H2O+O2↑.