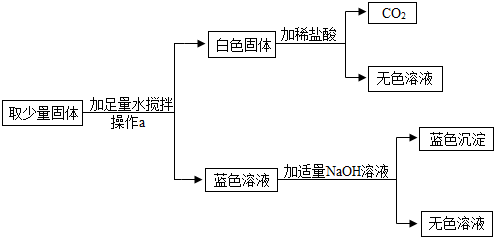
有一包固體粉末,可能由Ba(NO3)2、NaCl、Na2CO3、CuSO4、CaCO3、NaOH中的一種或幾種組成.現進行如下實驗:
(1)取少量該粉末,向其中加入足量水,充分攪拌后過濾,得到白色沉淀和無色濾液.
(2)在上述沉淀中加入足量稀鹽酸,沉淀全部溶解,并放出無色氣體.
(3)用pH試紙測得(1)中無色濾液pH為14.
(4)取少量(1)中無色濾液,加入適量稀硫酸,無明顯現象.
(5)另取少量(1)中無色濾液,加入稀硝酸和硝酸銀溶液,無白色沉淀產生.
根據以上現象,判斷該固體粉末的所有可能組成(可不填滿,也可補充):
第一組________;
第二組________;
第三組________;…
解:由(1)現象可得:混合物中一定不含硫酸銅.因硫酸銅溶液為藍色.
由(2)現象可得:混合物中可能含有碳酸鈣或碳酸鈉和硝酸鋇.
由(3)現象可得:溶液為堿性,所以溶液中可能含有氫氧化鈉和碳酸鈉中的一種或兩種.
由(4)現象可得:混合物中可能含有的碳酸鈉和硝酸鋇恰好完全反應,或不含碳酸鈉.
由(5)現象可得:混合物中一定不含氯化鈉.
由以上現象我們可得在混合物中一定不含:硫酸銅和氯化鈉.其它物質可能同時存在,也可能存在其中的一部分.若不含碳酸鈣時,硝酸鋇和碳酸鈉一定同時存在,且氫氧化鈉可能不存在,也可能存在.
故答案為:NaOH、CaCO3;
NaOH、Na2CO3、Ba(NO3)2;
NaOH、Na2CO3、Ba(NO3)2、CaCO3.
分析:在確定混合物的組成時,首先根據將混合物放入水中,出現的現象判斷一定含有哪種物質一定不會含哪種物質.然后再根據后面出現的現象進行判斷.
點評:碳酸鈣是一種不溶于水但能溶于酸的固體.同時,硝酸鋇和碳酸鈉生成的碳酸鋇也是一種不溶于水但是可以溶于酸的沉淀.所以在判斷時兩者都有可能存在.