
【題目】下圖是A物質(不含結晶水)的溶解度曲線.

(1)A物質的溶解度隨隨的升高而_____(選填“增大”、“減小”或“不變”.)
(2)在t2℃時,將15gA物質放入50g水中,攪拌,充分溶解后,形成的溶液溶質質量分數為_____;
(3)N點表示t3℃時A物質的_____(填“飽和”或“不飽和”)溶液;
(4)如下是M、N兩點代表的溶液相互轉化的途徑路線圖(“…>”表示轉化方向).
其中,采取“先將M點溶液加入一定量的水后,然后再升高溫度至N點對應的溫度”這一措施來實現M→N轉化的途徑路線圖是_____(填序號);根據甲圖來實現N→M轉化,應采取的措施是_____.

【答案】增大 20% 不飽和 丁 先將N點溶液降低溫度至M點對應的溫度,再向溶液中加入溶質固體或再恒溫蒸發溶劑 .
【解析】
(1)A物質的溶解度曲線隨溫度升高而上升,說明物質A的溶解度隨溫度升高而增大;
(2)t2℃時物質A的溶解度為25g,即100g水最多可以溶解25g物質A;現將15gA物質放入50g水中,攪拌充分溶解后,仍有15g﹣12.5g=2.5g固體A物質剩余而不能溶解,即此時所得溶液為該溫度下的飽和溶液,則所得溶液的溶質質量分數=![]() =20%;
=20%;
(3)N點位于物質A的溶解度曲線下方,表示此點所示溶液為不飽和溶液;
(4)M點為t2℃時物質A的飽和溶液,先將M點溶液加入一定量的水后,溶液溫度不變而加水變成了不飽和溶液,因此M點豎起下降;然后再升高溫度至N點對應的溫度,只升高溶液的溫度因此M點繼續向右平移至N點;此過程與丁圖所示一致;
甲圖所示,N點先平移再豎起向上移動至M,平移說明此時只是對溶液降溫,溶液組成不變;降溫后點仍位于曲線下方,仍為不飽和溶液,此時可通過增加溶質或恒溫蒸發溶劑,在不改變溫度的情況下,使點豎起上升至M而變成飽和溶液;
故答案為:(1)增大;(2)20%;(3)不飽和;(4)丁;先將N點溶液降低溫度至M點對應的溫度,再向溶液中加入溶質固體或再恒溫蒸發溶劑.


 發散思維新課堂系列答案
發散思維新課堂系列答案科目:初中化學 來源: 題型:
【題目】如圖是X、Y、Z三種液體的對應近似pH,下列判斷不正確的是( )

A. X顯酸性
B. Y一定是水
C. Z可能是某種鹽溶液
D. Z可使紫色石蕊試液變藍
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某實驗操作考試的題目是“配制20%的氯化鈉溶液70g”。該實驗的部分操作如下圖所示
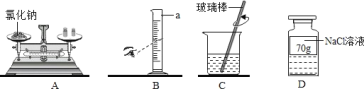
(1)A中需要稱取氯化鈉的質量是_____g,稱量時天平出現了右盤低的現象,接下來的操作是_____(填序號)
①左邊的平衡螺絲向左調②右邊的平衡螺絲向右調③右盤中減砝碼④左盤中加食鹽
(2)量取水時,如果按照圖B的方法讀數,會使配制的溶液溶質質量分數_____(填“偏大”或“偏小”)
(3)C中用玻璃棒攪拌的作用是_____
(4)D中所貼標簽有不妥之處,請在方框中填寫正確的標簽_____

(5)欲將10g20%的氯化鈉溶液配制為5%的氯化鈉溶液,需要加水的質量是_____g
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】小朱同學分別用溶質質量分數為3.65%、0.365%、0.0365%、0.00365%的稀鹽酸各30mL,分別與不同濃度的NaOH溶液反應,測定4個反應過程中的pH,繪制成如圖象。
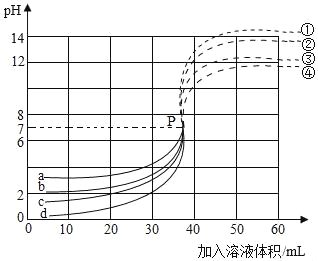
(1)寫出實驗時發生反應的化學方程式_____,用溶質質量分數為3.65%的稀鹽酸進行實驗時溶液溫度的變化是_____
(2)曲線c代表的實驗所用的是ω=_____的稀鹽酸,加入20 mLNaOH溶液時,溶液中主要存在的離子是_____(填離子符號)。
(3)曲線a代表的反應在P點后對應的曲線是_____(填①、②、③、④)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】請用化學用語填空:
(1)氬的元素符號_____。
(2)兩個亞鐵離子_____。
(3)標出碳酸鉀中碳元素的化合價_____。
(4)地殼中含量最多的元素_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】“讓我市菜子油飄香全國”菜子油中所含檸檬醛(化學式為C10H16O)能抑制黃曲霉菌的活性,對冠脈,心血管病有較好療效。下列關于檸檬醛敘述正確的是
A. 檸檬醛是由10個碳原子、16氫原子和1個氧原子構成
B. 檸檬醛是由碳、氫、氧三種元素組成的,但它不屬于氧化物
C. 檸檬醛中,碳、氫、氧元素的質量比為10:16:1
D. 檸檬醛中,氧元素的質量分數為16﹪
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】推理是學習化學的一種重要方法。下列推理合理的是( )
A. 離子是帶電的粒子,帶電的粒子一定是離子
B. 單質是由同種元素組成的,則只含一種元素的純凈物,一定是單質
C. 置換反應有單質和化合物生成,則有單質和化合物生成的反應,一定是置換反應
D. 溶液具有均一性和穩定性,則有均一性和穩定性的液體一定是溶液
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列有關敘述、對應方程式、基本反應類型都正確的是( )
A. 硝銨不能和熟石灰混用:2NH4NO3+Ca(OH)2=Ca(NO3)2+2H2O+2NH3↑復分解反應
B. 赤鐵礦煉鐵:![]() 置換反應
置換反應
C. 葡萄糖在人體中氧化:![]() 氧化反應
氧化反應
D. 比較鐵和銀的金屬活動性:Fe+2AgCl=FeCl2+2Ag置換反應
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(1)某研究性學習小組為驗證“氨氣還原氧化銅”的實驗,認真閱資料并做出以下準備。
資料準備:I.氨氣是一種無色、有刺激性氣味的氣體,密度比空氣小,極易溶于水,溶液呈堿性。
Ⅱ.氨氣還原氧化銅的化學反應原理:2NH3+3CuO![]() 3Cu+N2+3H2O。
3Cu+N2+3H2O。
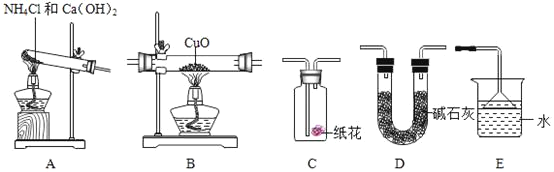
實驗準備:
請回答:
①為達成“氨氣還原氧化銅”的實驗目的,裝置A、B、D、E的正確連接順序_____;(填序號)
②裝置A中發生反應的化學方程式_____;
③裝置B觀察到的現象_____,裝置E的作用_____;
④將裝置A產生的氣體通入裝置C中,石蕊試液浸泡的紙花變藍色,原因是_____。
(2)金屬鎂可與熱水反應生成氫氧化鎂和氫氣,所得溶液呈堿性,可使酚酞溶液顯紅色。某同學將鎂條放在水中煮沸,趁熱取出部分溶液,滴加酚酞溶液,變為紅色,放置在空氣中一段時間后,發現溶液的紅色褪去了。
①鎂與熱水反應的化學方程式是_____。
②查閱資料:溶液紅色褪去的原因是溶液堿性減弱。
(提出問題)導致溶液堿性減弱的原因是什么?
(假設與分析)
假設1:可能是氫氧化鎂與N2或O2發生了反應。
假設2:可能是溶液吸收了空氣中的_____。
假設3:可能是氫氧化鎂的溶解度隨溫度的降低而_____。
由堿的性質可知,假設1不成立。
(實驗探究)
實驗操作 | 實驗現象 | 結論 |
(1)取上述紅色溶液,保持溫度不變,在空氣中放置一段時間,觀察現象。 | _____ | 假設2成立 |
(2)取上述紅色溶液,_____,_____,觀察現象。 | 紅色褪去 | 假設3成立 |
(拓展延伸)
③將一小塊金屬鈉投入硫酸銅溶液時,產生藍色沉淀。
請解釋其原因:_____。
④除上述金屬外,根據金屬活動性順序,預測_____也能跟硫酸銅溶液反應產生上述現象(舉一例即可)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com