
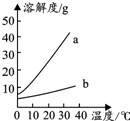
 如圖是Na2CO3、NaHCO3的溶解度表及溶解度曲線.
如圖是Na2CO3、NaHCO3的溶解度表及溶解度曲線. | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
分析 根據固體的溶解度曲線可以:①查出某物質在一定溫度下的溶解度,從而確定物質的溶解性,②比較不同物質在同一溫度下的溶解度大小,從而判斷飽和溶液中溶質的質量分數的大小,③判斷物質的溶解度隨溫度變化的變化情況,從而判斷通過降溫結晶還是蒸發結晶的方法達到提純物質的目的.
解答 解:(1)通過分析溶解度表中的數據可知,Na2CO3溶解度曲線為a;
(2)10℃時,碳酸鈉的溶解度是12.5g,所以在100g水中加入20g碳酸鈉固體,所形成的溶液中碳酸鈉的質量分數為$\frac{12.5g}{100g+12.5g}$×100%=11%;
(3)碳酸鈉的溶解度受溫度變化影響較大,所以實驗室中要除去Na2CO3固體中的少量NaHCO3的物理方法的操作步驟是:溶解,降溫結晶,過濾;
(4)已知Na2CO3轉化為NaHCO3的反應為Na2CO3+CO2+H2O═2NaHCO3,根據以上信息,要除去NaHCO3飽和溶液中的少量Na2CO3,應采用的化學方法是:通入足量的二氧化碳.
故答案為:(1)a;
(2)11%;
(3)降溫;
(4)通入足量的二氧化碳.
點評 本題難度不是很大,主要考查了固體的溶解度曲線所表示的意義,及根據固體的溶解度曲線來解決相關的問題,從而培養分析問題、解決問題的能力.


科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | CO2(CO):通過灼熱的氧化銅 | B. | KOH溶液(K2CO3):加適量稀鹽酸 | ||
| C. | Ba(NO3)2(BaCl2):溶于水過濾 | D. | 鋅粉(硫酸鋅粉末):加入足量稀硫酸 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com