
分析 根據質量守恒定律可知,反應前后固體的質量之差為氧氣的質量,然后將氧氣的質量代入化學反應方程式來計算氯化鉀的質量及二氧化錳的質量.
解答 解:(1)氯酸鉀與二氧化錳共熱生成氯化鉀和氧氣,所以反應前后減少的質量就是生成氧氣的質量,根據質量守恒定律可知生成氧氣的質量為15.5g-10.7g=4.8g;故填:4.8g;
(2)因加熱至完全反應,則10.7 g固體中含有氯化鉀和二氧化錳,.故填:氯化鉀;二氧化錳;
(3)設生成氯化鉀的質量為x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
149 96
x 4.8g
$\frac{149}{x}=\frac{96}{4.8g}$
解得x=7.45g
則剩余固體中MnO2的質量為10.7g-7.45g=3.25g
答:剩余固體中含有氯化鉀7.45g,含有二氧化錳3.25g.
點評 本題考查學生利用化學反應方程式的計算,明確質量守恒及氧氣為氣體來計算氧氣的質量是解答的關鍵,然后利用化學反應方程式來計算即可.


 名校課堂系列答案
名校課堂系列答案科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
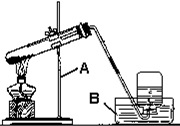 高錳酸鉀制取并收集氧氣的裝置如下:
高錳酸鉀制取并收集氧氣的裝置如下:查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 實驗步驟 | 實驗現象 | 實驗結論 |
| ①將適量黑色濾渣裝入試管中,再加入過氧化氫溶液 | 產生大量氣泡 | 有氣體生成 |
| ②立即向上述試管中伸入帶火星的木條 | 木條復燃 | 該氣體是氧氣 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
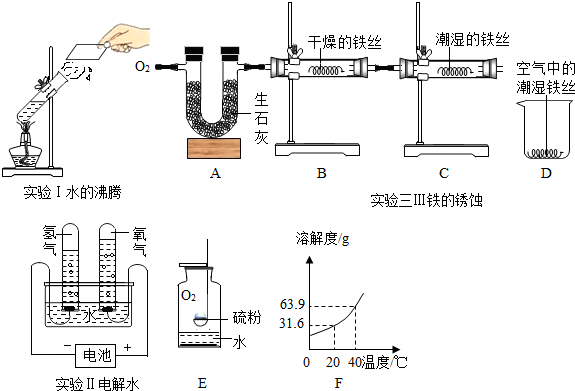
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

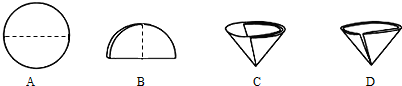
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com