
【題目】取鹽酸與氯化銅的混合溶液27g放入燒杯中,逐滴滴入質量分數為20%的NaOH溶液,產生沉淀質量與滴入NaOH溶液質量的關系如圖所示。

(1)滴入NaOH溶液的質量在0~4g時,發生反應的化學方程式為 ;
(2)與氯化銅反應的NaOH的質量為 g;
(3)原鹽酸與氯化銅的混合溶液中氯化銅的質量分數(寫出計算過程).
【答案】(1)HCl+NaOH=NaCl+H2O; (2)8g; (3)10%
【解析】
試題分析:
(1)向鹽酸與氯化銅的混合溶液滴入NaOH溶液,氫氧化鈉溶液先與稀鹽酸反應,將稀鹽酸完全反應后氫氧化鈉再與氯化銅反應生成沉淀。由圖像可知滴入NaOH溶液的質量在0~4g時,沒有出現沉淀,所以是鹽酸和氫氧化鈉的反應,鹽酸和氫氧化鈉反應生成氯化鈉和水: HCl+NaOH=NaCl+H2O;
(2)從圖象中的數據可以看出,從加入氫氧化鈉4g開始出現沉淀,到加入氫氧化鈉12g,沉淀開始不變,所以與氯化銅反應的NaOH的質量為12g﹣4g=8g;
(3)利用化學方程式,根據反應的質量比即可計算出氯化銅的質量。
設原鹽酸與氯化銅的混合溶液中氯化銅的質量為x,
CuCl2+2NaOH=Cu(OH)2↓+2NaCl
135 80
x 8g×20%
![]()
x=2.7g
所以原鹽酸與氯化銅的混合溶液中氯化銅的質量分數為:![]() ×100%=10%
×100%=10%
答:略


科目:初中化學 來源: 題型:
【題目】銅仁市地處武陵山區,石灰石資源豐富,某課外小組同學取該樣品12.0g于燒杯中,向盛有樣品的燒杯中加入足量一定溶質質量分數的稀鹽酸溶液充分反應,所用稀鹽酸質量(用X表示)和燒杯中剩余固體質量(用Y表示)如圖所示(石灰石的主要成分是碳酸鈣,雜質不溶于水也不與酸反應),請回答下列問題:
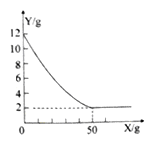
(1)石灰石中碳酸鈣的質量是多少?
(2)充分反應后共生成多少二氧化碳?
(3)所用稀鹽酸的溶質質量分數是多少?
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】根據提示猜猜下列描述的是何物質(寫名稱):
(1)“氣體,藍色火焰,能與血紅蛋白結合” ;
(2)“空氣老大,性格孤獨,保護燈泡” ;
(3)“似冰固體,致冷保鮮,人工降雨” .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列說法正確的是( )
A.原子的原子核都由質子和中子構成
B.稀有氣體元素的原子最外層都有8個電子
C.原子的質量主要集中在原子核上
D.地殼中含量最多的元素與生物細胞中含量最多的元素不相同
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列對分子、原子、離子的認識,正確的是( )
A.原子是一切變化中的最小粒子,不可再分
B.保持水的化學性質的最小粒子
C.分子、原子呈電中性,可以構成物質;離子帶有電荷,不能構成物質
D.原子失去電子形成陽離子,原子得電子形成陰離子
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(7分)某化學興趣小組在探究稀鹽酸的化學性質時,做了如圖一所示的三個實驗。
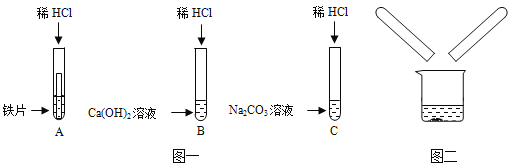
(1)寫出A試管中的反應現象 。
(2)寫出B試管中反應的化學方程式 。
(3)實驗結束后,小組同學將B、C兩支試管中的廢液同時倒入一個潔凈的燒杯中(如圖二所示),觀察到先有氣泡產生,后有白色沉淀生成。同學們將燒杯內的物質進行過濾,對所得濾液的溶質成分進行探究。
【提出猜想】
甲同學猜想:NaCl;
乙同學猜想:NaCl、CaCl2;
丙同學猜想:NaCl、CaCl2、 HCl;
你的猜想: 。
【交流討論】
你認為 同學的猜想一定不正確,理由是 。
【設計實驗】請設計實驗證明你的猜想正確。
實驗步驟 | 實驗現象 | 實驗結論 |
取少量濾液于試管中,向其中滴加 。 | 猜想成立 |
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖所示能正確反映其對應敘述的是
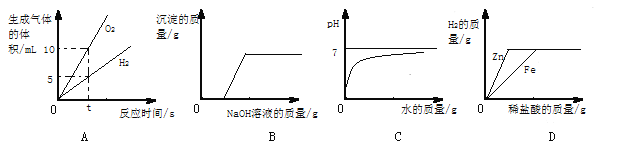
A.電解水一段時間
B.向氯化銅和鹽酸的混合物中滴加氫氧化鈉溶液
C.向硫酸溶液中不斷加水
D.向等質量的鋅和鐵中加入足量的稀鹽酸
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com