
分析 (1)根據化合物中各元素質量比=各原子的相對原子質量×原子個數之比,進行分析解答.
(2)化合物中元素的質量分數=$\frac{相對原子質量×原子個數}{相對分子質量}$×100%,據此進行分析解答.
(3)根據化合物中某元素的質量=該化合物的質量×該元素的質量分數,進行分析解答.
解答 解:(1)硝酸銨中氮、氧元素的質量之比是(14×2):(16×3)=7:12.
故答案為:7:12.
(2)尿素中氮元素的質量分數為$\frac{14×2}{12+16+(14+1×2)×2}$×100%≈46.7%.
故答案為:46.7%.
(3)解:設需要硝酸銨(NH4NO3)的質量為x,則x×$\frac{14×2}{14×2+1×4+16×3}$×100%=30噸×$\frac{14×2}{12+16+(14+1×2)×2}$×100%
x=40噸
答:40噸硝酸銨中氮元素的質量和30噸尿素中氮元素質量相等.
點評 本題難度不大,考查同學們靈活運用化學式的有關計算進行分析問題、解決問題的能力.


 優加精卷系列答案
優加精卷系列答案科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
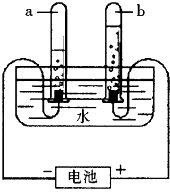 如圖所示的是電解水實驗裝置,通電一段時間后,在兩個試管中分別收集到氣體a和氣體b,請回答.
如圖所示的是電解水實驗裝置,通電一段時間后,在兩個試管中分別收集到氣體a和氣體b,請回答.查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 實驗室用加熱高錳酸鉀的方法制取氧氣,有如下操作步驟:
實驗室用加熱高錳酸鉀的方法制取氧氣,有如下操作步驟:| A. | ②①④⑤③⑥ | B. | ②①④⑤⑥③ | C. | ①②④⑤⑥③ | D. | ①②④⑤③⑥ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com