
【題目】如圖是甲、乙兩種物質的溶解度曲線,請回答下列問題。
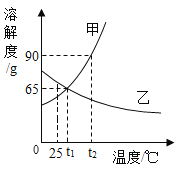
(1)_°C 時,甲、乙兩種物質的溶解度相等。
(2)將乙的飽和溶液變成不飽和溶液的方法是_。(任寫一種)
(3)t2°C時,分別將甲、乙兩種物質的飽和溶液降溫到t1°C,有晶體析出的是__,此時甲溶液的溶質質量分數_(填“大于”、“等于”或“小于”)乙溶液的溶質質量分數。
(4)小明同學用20ml 水(密度約為1g/ml )配制t1°C的甲飽和溶液:
①計算需要稱量的甲的質量是____g。
②將稱取的甲固體和20ml水倒入燒杯中,_(填操作名稱),直至固體完全溶解。
【答案】t1 加水或降低溫度 甲 大于 13 攪拌
【解析】
(1)據圖可以看出,在t1℃時,甲、乙兩種物質的溶解度相等,故填:t1;
(2)乙的溶解度隨溫度的升高而減小,要將乙的飽和溶液變成不飽和溶液可以采用加水或降低溫度的方法,故填:加水或降低溫度;
(3)甲的溶解度隨溫度降低而減小,乙的溶解度隨溫度降低而增大,所以t2℃時,分別將甲、乙兩種物質的飽和溶液降溫到t1℃,甲有晶體析出;乙的溶解度變大,溶質質量分數與降溫前相等,據飽和時質量分數的計算式![]() ×100%,即溶解度越大質量分數也就越大,而t1℃甲的溶解度大于t2℃乙的溶解度,所以此時甲溶液的溶質質量分數大于乙溶液的溶質質量分數。故填:甲;大于;
×100%,即溶解度越大質量分數也就越大,而t1℃甲的溶解度大于t2℃乙的溶解度,所以此時甲溶液的溶質質量分數大于乙溶液的溶質質量分數。故填:甲;大于;
(4)①20ml水即20g水,t1℃時甲的溶解度為65g,即100g水中溶解65g甲剛好可以得到飽和溶液,所以20g水需要甲的質量為65g×![]() =13g。故填:13;
=13g。故填:13;
②將稱取的甲固體和20ml水倒入燒杯中,用玻璃棒攪拌,直至固體完全溶解。故填:攪拌。


科目:初中化學 來源: 題型:
【題目】根據如圖所示裝置,回答有關問題:
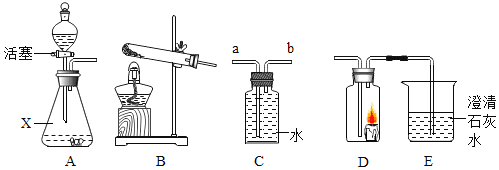
(1)裝置A中,儀器X的名稱為______,其中用分液漏斗代替長頸漏斗的優點是______。
(2)實驗室常用氯酸鉀制取氧氣,發生裝置應選擇______![]() 填字母
填字母![]() ,反應的化學方程式是______
,反應的化學方程式是______
(3)若用裝置C收集氫氣,則氫氣應從______![]() 填“a”或“b”
填“a”或“b”![]() 端導管口通入。
端導管口通入。
(4)乙炔是一種微溶于水的氣體,密度與空氣接近,實驗室常用塊狀電石和水在常溫下反應制取乙炔,故制取乙炔的發生裝置選______。![]() 填裝置序號
填裝置序號![]()
(5)某同學點燃蠟燭,然后放入D中,迅速連接A、D、E,打開活塞進行實驗,發現E中溶液逐漸變渾濁,則裝置A中產生的氣體______。![]() 填“一定”或“不一定”
填“一定”或“不一定”![]() 為二氧化碳氣體。
為二氧化碳氣體。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】石膏(CaSO42H2O)是一種用途廣泛的工業材料和建筑材料,工業上用含SO2的煙氣制備石膏的簡要流程圖如下:
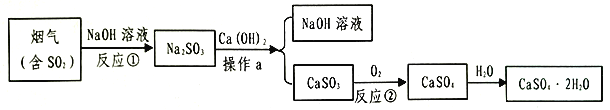
(1)在反應①時,常將NaOH噴成霧狀的原因是___________________.
(2)操作a的名稱是__________,在實驗室里進行該操作,玻璃棒的作用是__________.
(3)CaSO3不易溶于水,它屬于________(填“酸”、“堿”、“鹽”或“氧化物”),其中硫元素的化合價為________,反應②的化學方程式是_________________________.
(4)生產流程中生成的______________可循環利用,節約成本.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】“眾志成城戰疫情”,在抗擊新型冠狀病毒引發的肺炎疫情中大量使用84消毒液來進行消毒,84消毒液的主要成分是次氯酸鈉(NaC1O)。下列關于次氯酸鈉的說法中不正確的是( )
A.次氯酸鈉中氯元素的化合價為+5價
B.次氯酸鈉中氧元素的質量分數最小
C.次氯酸鈉中鈉、氯、氧三種元素的質量比為46:71:32
D.次氯酸鈉由鈉、氯、氧三種元素組成
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】結合下圖實驗裝置,回答有關問題:

(1)指出圖中a儀器的名稱:_____。
(2)用高錳酸鉀固體制取較純凈的氧氣,選用的裝置是____,反應的化學方程式為_____。
(3)實驗室制取二氧化碳時,若用E裝置干燥二氧化碳,則E中應盛放____,氣體應從____(填“c”或“d”)端通入,若發生裝置選用C裝置來制取該氣體,其優點是_____。
(4)二氧化氯(C1O2)用作消毒劑,C1O2是一種橙黃色,有刺激性氣味的氣體,11°C以下為紅色氣體,易溶于水,見光易分解。可用粉末狀固體氯酸鈉(NaC1O3)與濃鹽酸反應制取C1O2,反應的化學方程式為:2NaClO3+4HCl=2ClO2↑+Cl2↑+2X+2NaCl
①制取C1O2氣體的發生裝置應選用______(填裝置序號)裝置。
②上述反應中X的化學式為_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】硼泥主要由MgO 和SiO2 組成,含有少量Fe2O3 、FeO 、Al2O3 等雜質。用硼泥生產氫氧化鎂的工藝流程如圖所示:
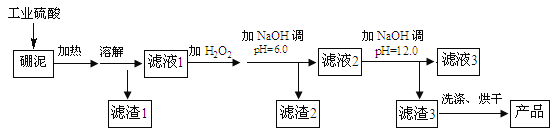
提示信息:
Ⅰ.加入H2O2的目的是將溶液中 Fe2+氧化為 Fe3+
Ⅱ.SiO2不與硫酸反應
Ⅲ.已知某些金屬陽離子在溶液中生成氫氧化物沉淀的pH如下表所示,當溶液的pH達到完全沉淀值時,可以認為金屬陽離子已完全沉淀。
氫氧化物 | 完全沉淀時的pH |
Mg(OH)2 | 10.8 |
Fe(OH)2 | 9.6 |
Fe(OH)3 | 3.7 |
Al(OH)3 | 4.7 |
(1)寫出加熱溶解中發生反應的其中一個化學方程式:____。
(2)濾液2中大量存在的金屬離子是___。
(3)調節兩次pH值的原因是___。
(4)利用Mg(OH)2與含SO2和O2的煙氣反應生成MgSO4和另一種無污染的化合物,可以使煙氣脫硫,請問另一種產物的化學式為___。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗室制取氣體所需裝置如下圖所示。
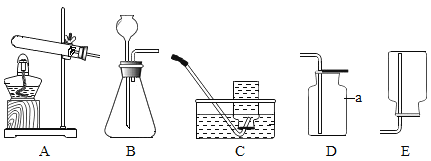
請回答以下問題:
(1)裝置中標“a”的儀器名稱是_____。
(2)用高錳酸鉀制取氧氣時,所選用的發生裝置是_____,收集裝置是C或_____。(填字母序號,下同)
(3)用大理石和稀鹽酸制取二氧化碳時,所選用的發生裝置是_____。該裝置還可用于制氧氣,其反應的化學方程式為_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】分類和類比是學習化學常用的方法。
(1)下列實驗都能探究酸與堿之間能否發生反應。請從“定性研究”或“定量研究”的角度,將下列實驗中的A與_________(填字母)歸為一類,理由是_____________。
|
在少量的氫氧化銅固體中加入足量的稀鹽酸 |
在氫氧化鈉溶液不斷滴加稀硫酸,邊加邊用酸度計測定溶液的pH |
A | B | C |
(2)非金屬與氫氣反應的條件越容易、反應越劇烈,則非金屬元素的非金屬性越強。據此規律,可推斷出第三周期非金屬元素的非金屬性強弱的順序為__________________;結構決定性質,請歸納位于第三周期元素的原子結構與元素性質的遞變規律______________________。
元素 | Si | p | S | Cl |
單質與氫氣的反應條件 | 高溫 | 磷蒸氣與氫氣能反應 | 加熱 | 加熱或點燃時發生爆炸 |
原子核外電子排布 |
|
|
|
|
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】化學用語是學習化學的重要工具。下面對化學用語含義的敘述正確的是( )
①H ②Fe ③![]() ④
④![]() ⑤2MgO
⑤2MgO
A. ③表示鐵離子
B. 能表示一個分子的有④⑤
C. ②和③屬于同種元素
D. ④表示![]() 由1個碳元素和2個氧元素組成
由1個碳元素和2個氧元素組成
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com