
【題目】為探究影響鐵和鹽酸反應速率的因素,興趣小組利用傳感器測定氫氣濃度隨時間的變化,如下表所示。每一個實驗在其他條件不變時,下列說法不正確的是
圖象 |
|
|
|
實驗 | 等質量的鐵絲、鐵粉分別與相同濃度的鹽酸反應 | 等質量的鐵粉分別與不同濃度的鹽酸(3%和1.5%)反應 | 不同溫度下, 等質量的鐵粉與相同濃度的足 量稀鹽酸反應 |
A.由圖1可知鐵粉反應更快
B.由圖1可得結論:鹽酸不能與鐵絲反應
C.由圖2可知3%的鹽酸與鐵粉反應更快
D.由圖3所示實驗可知溫度不影響生成氫氣的總質量
科目:初中化學 來源: 題型:
【題目】鈦金屬具有硬度大、熔點高、常溫下耐酸堿、耐腐蝕等優良的性能,被譽為“未來金屬”。我國釩鈦磁鐵礦床分布廣泛,儲量豐富,由釩鈦磁鐵礦提取金屬鈦的主要工藝過程如下:
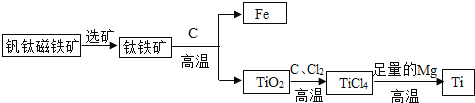
(1)鈦鐵礦的主要成分為鈦酸亞鐵,鈦酸亞鐵的化學式FeTiO3,其中鈦的化合價為_____價。
(2)TiCl4在高溫下與足量Mg反應生成金屬Ti,該反應的化學方程式_____。則上述生產過程中得到的金屬鈦中混有少量金屬雜質,可加入_____除去。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】口罩是抗擊“新冠病毒”的重要物資,其核心材料是熔噴布, 它是以聚丙烯(CH2CHCH3)n超細纖維為主要原料制成的 高靜電過濾材質,具有很好的空氣過濾性。目前,市售口罩 主要有 N95 系列口罩、醫用外科口罩等。下列有關說法中, 不正確的是( )

A.熔噴布主要原料聚丙烯屬于有機高分子材料
B.口罩可以阻擋空氣中所有的氣體和顆粒物
C.口罩短暫使用后應及時通風晾干,但不能洗滌后重復使用
D.廢棄口罩可用塑料袋密封好,放入指定有毒有害垃圾桶內
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列實驗現象描述錯誤的是( )
A.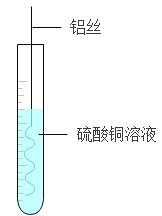 鋁絲浸入硫酸銅溶液中:銀白色固體表面覆蓋一層紫紅色固體,藍色溶液逐漸變為無色
鋁絲浸入硫酸銅溶液中:銀白色固體表面覆蓋一層紫紅色固體,藍色溶液逐漸變為無色
B. 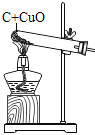 木炭還原氧化銅:黑色粉末逐漸變為紫紅色
木炭還原氧化銅:黑色粉末逐漸變為紫紅色
C. 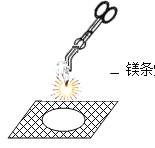 鎂條燃燒:銀白色固體燃燒,發出耀眼的白光,放熱,產生白煙,生成白色固體
鎂條燃燒:銀白色固體燃燒,發出耀眼的白光,放熱,產生白煙,生成白色固體
D.  焚燒含氯塑料:產生有刺激性氣味的氯化氫氣體
焚燒含氯塑料:產生有刺激性氣味的氯化氫氣體
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為了測定某黃銅樣品中銅的質量分數,某化學小組進行了如下實驗:
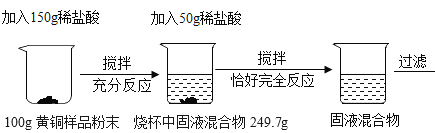
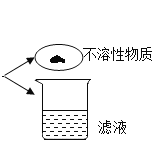
請回答下列問題:
(1)上述實驗過程中發生反應的化學方程式為_____;
(2)根據已知條件列出求解第一次所加的稀鹽酸中溶質質量(x)的比例式_____;
(3)此黃銅樣品中銅的質量分數為_____;
(4)用 36.5%的濃鹽酸配制 200g 上述稀鹽酸,所需濃鹽酸的質量為_____g;
(5)若將反應后的濾液蒸發掉 12.6g 水,所得不飽和溶液中溶質的質量分數為_____;
(6)欲將黃銅樣品中的銅轉化為銅鹽,可將過濾后所得固體洗滌、烘干,然后在空氣中加熱,充分反應,可得到氧化銅的質量是_____g,再經過某些反應及操作就得到了所 需銅鹽。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】甲烷和水蒸氣在反應器中經催化重整可制得較高純度的氫氣。
(1)初始反應如下,請補全反應。
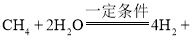 ____________
____________
(2)反應器中還存在其他化學反應。
①其中一個反應的微觀示意圖如下,依據質量守恒定律,在方框內補全相應微粒的圖示__________。
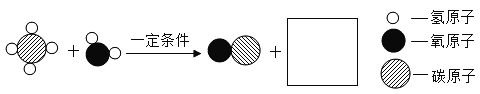
②另外兩個反應: i.  ,ii.
,ii.  。反應i中若制得200gH2,至少需要CO的質量為____________g;反應ii屬于_____________(填基本反應類型)。
。反應i中若制得200gH2,至少需要CO的質量為____________g;反應ii屬于_____________(填基本反應類型)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】豆漿的營養價值很高,是人們喜愛的飲品之一。豆漿中含有豐富的植物蛋白、磷脂、維生素A、維生素C、煙酸和鐵、鈣等礦物質,其中鈣的含量比其他乳類還要豐富。則:
(1)每天早上喝上一杯豆漿,這說明豆漿可為我們補充的主要營養物質是(______)
A 蛋白質 B 油脂 C 維生素 D 無機鹽
(2)豆漿機即需即制的優點給生活帶來很大方便,豆漿制作完成,還可用隨機附件——濾網去除豆漿中的渣滓,使口感更好,該設計利用的操作原理是_______。
(3)黃豆中含有的皂角素能引起人們惡心、嘔畦和消化不良,因此,喝不熟豆漿對人體有害。但豆漿經燒熟煮透后,其中的有害物質即被破壞,這個過程發生的是____變化(填“物理”或“化學”);纖維素的化學式為(C6H10O5)n,在催化劑和加熱的條件下纖維素可以與水反應生成葡萄糖,寫出該反應的化學方程式為________。
(4)小明同學通過化學課知道,人們誤食重金屬鹽(如:硫酸銅、氯化鋇等)可通過喝大量豆漿的方法解毒。你認為下列______飲品也可以達到同樣的目的(填序號)。
①牛奶;②果汁;③蛋清;④礦泉水;⑤食鹽水。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】我國是世界鋼鐵產量最大的國家,煉鐵的主要原料是鐵礦石。用赤鐵礦石(主要成分為Fe2O3)煉鐵的反應原理為:Fe2O3+3CO![]() 2Fe+3CO2。
2Fe+3CO2。
(1)上述反應不是置換反應的理由是:_____________________________。
(2)根據化學式計算:Fe2O3中鐵元素的質量分數____。
(3)根據化學方程式計算:用含Fe2O3 60%的赤鐵礦石800 t,理論上可煉出純鐵多少噸____?
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】現有等質量X,Y的兩種金屬,分別放入溶質質量分數相同的足量稀硫酸中,產生氫氣的質量與反應時間的關系如圖所示(已知X,Y在生成物中化合價均為+2價).則下列說法不正確的是( )
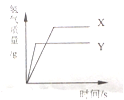
A. 生成氫氣的質量:X>Y B. 相對原子的質量:X>Y
C. 金屬活動性:Y>C D. 消耗硫酸的質量:X>Y
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com