
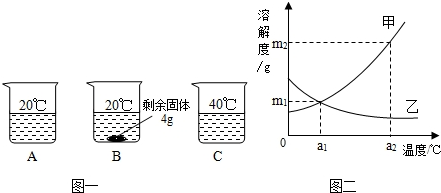
向分別裝有50g水的A、B、C燒杯中加入10g、20g、30g的KNO3固體,充分溶解后,現象如圖一所示: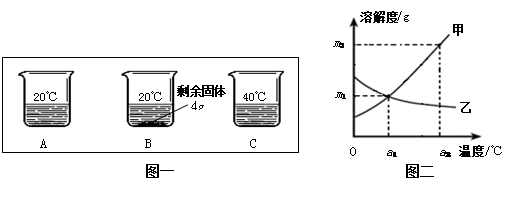
(1)A、B、C燒杯中溶液一定屬于飽和溶液的是_______(選填序號)。
(2)圖二中 (選填“甲”或“乙”)能表示KNO3溶解度曲線。
(3)KNO3在20℃時溶解度等于 。
(4)要使B燒杯中剩余固體繼續溶解,可采用的方法是_________________________;
(5)由圖二分析,若分別將甲、乙100g的飽和溶液從a2℃降溫到a1℃,無晶體析出的是 (選填“甲”、 “乙”或“甲和乙”),比較降溫后所得溶液中溶質的質量分數甲 乙(選填“>”或“<”或“=”)
(6)若要使a1℃時含100g水的甲的飽和溶液變為a2℃的飽和溶液(溶劑的量不減少),應采取的措施為 (請依據圖示作定量描述)。
(1)B (2)甲 (3)32g (4)加水(或答“升高溫度”) (5)乙 >
(6)加入(m2-m1)g固體甲,并升高溫度至a2℃
解析試題分析:(1)依據飽和溶液的概念可知,B燒杯中有固體未溶解,即在此溫度下,不能繼續溶解該物質,故一定是飽和溶液;
(2)由于硝酸鉀的溶解度隨溫度的升高而增大,故曲線甲能表示KNO3溶解度曲線;
(3)根據題意,在盛有50g水的B燒杯中加入20g的KNO3固體,有4g未溶解,即在50g水中溶解了16gKNO3固體而達到飽和,故KNO3在20℃時的溶解度=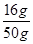 ×100g=32g;
×100g=32g;
(4)由于硝酸鉀的溶解度隨溫度的升高而增大,所以要使B燒杯中的固體繼續溶解,可采取的方法是升高溫度或增加溶劑;
(5)根據溶解度曲線可知,將甲、乙100g的飽和溶液從a2℃降溫到a1℃時,甲的溶解度減小,析出晶體;乙的溶解度增大,溶液變為不飽和溶液,故不會析出晶體;降溫到a1℃時,由于有晶體析出,故甲仍是飽和溶液,其溶質質量分數=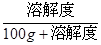 ×100%;溫度從a2℃降溫到a1℃時,由于乙變成不飽和溶液,故溶質質量分數小于
×100%;溫度從a2℃降溫到a1℃時,由于乙變成不飽和溶液,故溶質質量分數小于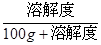 ×100%,而a2℃時甲、乙的溶解度相等,所以可得出該溫度時,所得溶液溶質質量分數甲大于乙;
×100%,而a2℃時甲、乙的溶解度相等,所以可得出該溫度時,所得溶液溶質質量分數甲大于乙;
(6)由于甲物質的溶解度隨溫度的升高而增大,且a1℃時的溶解度為m1,a2℃時的溶解度為m2,故若要使a1℃時含100g水的甲的飽和溶液變為a2℃的飽和溶液(溶劑的量不減少),應采取的措施為:加入(m2-m1)g固體甲,并且升高溫度至a2℃。
考點:飽和溶液與不飽和溶液,飽和溶液和不飽和溶液相互轉變的方法,固體溶解度曲線及其作用,溶質的質量分數、溶解性和溶解度的關系
點評:本題難度不是很大,主要考查了固體溶解度曲線所表示的意義及根據溶解度曲線來解決相應的問題,解 題的關鍵是要熟記和理解固體溶解度曲線及其應用,并能靈活運用于實際問題的解答。


科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源:2012-2013學年天津市河西區九年級上學期期末考試化學試卷(解析版) 題型:填空題
向分別裝有50g水的A、B、C燒杯中加入10g、20g、30g的KNO3固體,充分溶解后,現象如圖一所示:

(1)A、B、C燒杯中溶液一定屬于飽和溶液的是_______(選填序號)。
(2)圖二中 (選填“甲”或“乙”)能表示KNO3溶解度曲線。
(3)KNO3在20℃時溶解度等于 。
(4)要使B燒杯中剩余固體繼續溶解,可采用的方法是_________________________;
(5)由圖二分析,若分別將甲、乙100g的飽和溶液從a2℃降溫到a1℃,無晶體析出的是 (選填“甲”、 “乙”或“甲和乙”),比較降溫后所得溶液中溶質的質量分數甲 乙(選填“>”或“<”或“=”)
(6)若要使a1℃時含100g水的甲的飽和溶液變為a2℃的飽和溶液(溶劑的量不減少),應采取的措施為 (請依據圖示作定量描述)。
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源:2012-2013學年天津市河西區九年級(上)期末化學試卷(解析版) 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com