
鐵及其化合物在生活生產中有重要的應用。請回答下列問題:
(1)鐵制品在空氣中易銹蝕,其實質是鐵與空氣中的氧氣、 等接觸后發生化學反應的過程。
(2)在盛有氧氣的集氣瓶中點燃細鐵絲發生劇烈燃燒的化學方程式是 。為防止集氣瓶破裂,常采取的措施是 。
(3)把鐵粉和銅粉的混合物放入硝酸銀溶液中,充分反應后,過濾,為確定濾渣和濾液 的成分,甲同學向濾渣中滴加稀鹽酸,無氣泡產生; 乙同學向濾
的成分,甲同學向濾渣中滴加稀鹽酸,無氣泡產生; 乙同學向濾 液中滴加稀鹽酸,產生白色沉淀。根據兩同學實驗的現象,分析下列結論不正確的是 (填寫字母序號)。
液中滴加稀鹽酸,產生白色沉淀。根據兩同學實驗的現象,分析下列結論不正確的是 (填寫字母序號)。
A.濾渣中只含銀 B.濾渣中一定含 有銀,可能含有銅
有銀,可能含有銅
C.濾液中一定有Ag+ 、Fe2+ 和Cu2+ D.濾液中只含Ag+ 和Fe2+,不含Cu2+
【探究】廢舊金屬的回收利用。
廢鐵屑的主要成份是鐵,同時還有少量鐵銹(Fe2O3),生產動物飼料添加劑硫酸亞鐵的工藝之一如下圖所示:
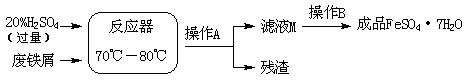 |
(4)在反應器中發生反應的化學方程式有:
Fe + H2SO4 =FeSO4 +H2↑、 、 Fe2(SO4)3 + Fe = 3FeSO4。
(5)濾液M中肯定含有的溶質的化學式是 ;
(6)在化學反應中,凡是有元素化合價變化的反應屬于氧化還原反應。下列反應類型肯定屬于氧化還原反應的是 (填字母編號);
A.化合反應 B.置換反應 C.分解反應 D.復分解反應
(7)取表面含有氧化鎂的鎂條(無其它雜質)2.5g,加入到足量的20.0g的稀硫酸中,充分反應后,所得溶液的質量為22.3g。求:該鎂條中單質鎂的質量分數。(計算過程寫在答卷紙對應的位置)
(1)水(或水蒸氣或H2O)
(2)3Fe + 2O2 點燃 Fe3O4 在集氣瓶底放少量水(或沙子)
(3)BD (4)Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
(5)FeSO4 、H2SO4 (6)B
(7)(3分)[解]設: 2.5g鎂條樣品中單質鎂的質量為X
反應產生的氫氣質量:2.5g + 20.0g - 22.3g = 0.2g (0.5分)
Mg+H2SO4 = MgSO4+H2↑
24 2
X 0.2g
24/2 = X/0.2g X = 2.4g (1分)
該鎂條中單質鎂的質量分數 = 2.4g / 2.5g X 100% = 96% (1分)
答:該鎂條中單質鎂的質量分數為96%。  (設及答 合計0.5分,缺一不得分)
(設及答 合計0.5分,缺一不得分)


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:
將金屬X置于氯化鋁溶液中,X表面無固體析出;而將其置于硝酸銀溶液中,會發生反應:X +2 AgNO3 === X(NO3)2 +2Ag 。由此可判斷X、Al、Ag的金屬活動性順序為
A.Al﹥Ag﹥X B.Ag﹥X﹥Al C.Al﹥X﹥Ag D.X﹥Al﹥Ag
查看答案和解析>>
科目:初中化學 來源: 題型:
為除去下列物質中的雜質(括號內為雜質),下列操作方法能達到目的的是
| 選項 | 物質(雜質) | 操作方法 |
| A | CO2(H2O) | 將氣體通過盛有火堿的干燥 |
| B | Cu(CuO) | 通入足量氧氣并加熱 |
| C | Na2SO4(Na2CO3) | 加鹽酸至恰好不再產生氣泡為止 |
| D | FeCl2(CuCl2) | 加入足量鐵 |
查看答案和解析>>
科目:初中化學 來源: 題型:
現代客機外地殼主要材料是鋁鋰合金。鋰的原子結構示意圖為,下列關于鋰的說的說法錯誤的是
A.鏗元素屬于金屬元素
B.鏗原子的質子數為3
C.鏗元素在化合物中通常顯+3價
D.銼原子在化學反應中容易失去電子
查看答案和解析>>
科目:初中化學 來源: 題型:
實驗室許多藥品都需密封保存,下列對藥品密封保存原因的解釋,錯誤的是
A.濃鹽酸——防止揮發 B.NaOH溶液——防止與CO2反應
C.濃硫酸——防止吸水 D.生石灰——防止與氧氣反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com