
【題目】小成同學做完“用稀鹽酸和石灰石反應制取二氧化碳”的實驗之后,想進一步探究:是否可以測得實驗所用的石灰石中碳酸鈣的含量?又進行了如下實驗: ①將試管中反應的剩余物過濾并多次用蒸餾水洗滌,得到濾液和濾渣.
②向濾渣中滴加稀鹽酸,無明顯的現象.
③將濾渣干燥后稱量,質量為0.5g.
④向濾液中加入10%的Na2CO3溶液,獲得了相關的數據,并繪制成如圖所示的圖象.
根據實驗過程回答下列問題.(假設石灰石中的其余雜質不與稀 鹽酸反應)
(1)第①步中如果在過濾時沒有用蒸餾水多次洗滌,則測得碳酸鈣的質量分將 . (選填“偏大”、“不變”或“偏小”)
(2)第②步中小明向濾渣中加入稀鹽酸的目的是為了 .
(3)在Na2CO3溶液加到圖象中顯示的C點時,溶液中所含的溶質為 .
(4)根據圖象及相關的數據石灰石中碳酸鈣的質量分數.
【答案】
(1)偏小
(2)檢驗濾渣中是否含有碳酸鈣
(3)氯化鈉、氯化鈣
(4)解:設碳酸鈣質量為x,
由CaCO3+2HCl═CaCl2+H2O+CO2↑,Na2CO3+CaCl2═CaCO3↓+2NaCl可知,CaCO3~Na2CO3,
CaCO3~ | Na2CO3 |
100 | 106 |
x | (31.2g﹣10g)×10% |
![]() =
= ![]() ,
,
x=2g,
石灰石中碳酸鈣的質量分數為: ![]() ×100%=80%
×100%=80%
【解析】解:(1)第①步中如果在過濾時沒有用蒸餾水多次洗滌,會導致雜質質量偏大,從而導致測得碳酸鈣的質量分數偏小. 故填:偏小.(2)第②步中,向濾渣中加入稀鹽酸,如果產生氣泡,說明碳酸鈣沒有完全反應,如果不產生氣泡,說明碳酸鈣已經完全反應,因此目的是為了檢驗濾渣中是否含有碳酸鈣.
故填:檢驗濾渣中是否含有碳酸鈣.(3)在Na2CO3溶液加到圖象中顯示的C點時,溶液中所含的溶質為稀鹽酸和碳酸鈉反應生成的氯化鈉和碳酸鈉和氯化鈣反應生成的氯化鈉及其反應生成的氯化鈣.
故填:氯化鈉、氯化鈣.
【考點精析】認真審題,首先需要了解根據化學反應方程式的計算(各物質間質量比=系數×相對分子質量之比).


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:
【題目】如果把自然界水里溶解的氣體收集起來,結果是氧氣的體積分數大于21%,而氮氣的體積分數小于78%。此現象說明( )。
A. 空氣中氧氣的體積分數本來就大于21%,氮氣本來就小于78%
B. 空氣中氧氣的體積分數本來就小于21%,氮氣本來就大于78%
C. 氧氣比氮氣更難溶于水
D. 氧氣比氮氣更易溶于水
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某科學實驗小組想探究鹽酸、氫氧化鈣的化學性質,取8支試管分別用A﹣H 編號后,做如下實驗: 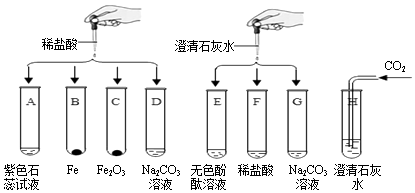
(1)實驗中觀察到有氣泡出現的試管是 , 有沉淀生成的試管是 .
(2)實驗后某試管的底部有白色固體,過濾后向濾液中滴加鹽酸,有氣泡冒出,則該濾液中的溶質是 .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列物質分別和36.5g20%的鹽酸恰好完全反應后,所得溶液中溶質質量分數最小的是
A. Mg B. MgO C. Mg(OH)2 D. MgCO3
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】甲、乙兩組同學分別設計了如下實驗,圖中試劑混合前后物質的總質量分別表示為M(前)、M(后). 
請根據圖示回答:
(1)甲組實驗中,M(前)>M(后),原因是;若所用試劑不變,改進的方法是;
(2)乙組實驗中,M(前)=M(后),丙組同學認為該實驗不能驗證質量守恒定律,原因是 .
(3)丁組同學研究了物質W的組成.一定條件下,W在密閉容器內發生反應前后各物質的質量如下圖所示: 
其中,x=g,W的化學式是 . (按碳、氫、氧元素順序書寫)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列化學方程式中符合題意且書寫正確的是( )
A.正常雨水偏弱酸性原因:SO2+H2O═H2SO4
B.生活中用天然氣作燃料:C2H3OH+3O2 ![]() 2CO2+3H2O
2CO2+3H2O
C.用小蘇打治療胃酸過多癥:NaHCO3+HCl═NaCl+CO2↑+H2O
D.工業上用熟石灰制取燒堿:Ca(OH)2+2NaNO3═Ca(NO3)2+2NaOH
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗桌上有一瓶無色液體,某同學說可以往溶液樣品中滴加石蕊試液,判斷其酸堿性。該環節屬于科學探究的( )
A. 提出問題 B. 作出猜想 C. 設計實驗 D. 反思評價
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com