
【題目】化學與生活息息相關。請根據已學的化學知識回答下列問題:
(1)大米中含有的主要營養素是(填名稱)____;
(2)選用鋁合金做飛機機身而不選用純鋁,主要原因是鋁合金硬度和強度_______(填“大于”或“小于”)純鋁。
(3)在家庭使用的凈水器里加入活性炭,是利用活性炭的_____性。
(4)用化學方程式表示稀硫酸除鐵銹的原理 _______。
科目:初中化學 來源: 題型:
【題目】興趣小組同學為了測定某中碳酸鈣的質量分數,稱取25.0g珍珠粉樣品,進行四次高溫煅燒、冷卻、稱量剩余固體的重復操作(雜質不參加反應),記錄數據如下:
操作次數 | 第1次 | 第2次 | 第3次 | 第4次 |
剩余固體質量(g) | 21.6 | 19.2 | 16.2 | 16.2 |
試計算:
(1)完全反應后生成二氧化碳的質量是__g。
(2)求珍珠粉中碳酸鈣的質量分數。(寫出計算過程)__________.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】一個興趣小組同學們在一起探究金屬及金屬礦物的性質,做了如下實驗。
(1)探究鋁、鐵、銅三種金屬的活動性,小剛同學設計了用銅絲、鐵絲、鋁絲和稀鹽酸,只用一只試管,取一次鹽酸的探究方案。請你和他們一起完善下表的探究方案并回答有關問題。
實驗步驟 | 觀察到的現象 |
①在試管中取少量鹽酸,插入銅絲,充分作用。 | 無明顯現象 |
②在①所得的溶液中,插入鐵絲,充分作用。 | _____ |
③在②所得的溶液中插入鋁絲,充分作用。 | _____ |
結論:金屬活動性由強到弱的順序_______。
(2)小明同學將鋁片、鋅片打磨后,分別投入盛有等體積、等濃度稀鹽酸的試管中,觀察到鋁與稀鹽酸反應較鋅與稀鹽酸反應快。
(提出問題)金屬與鹽酸反應快慢,除與金屬的種類有關外,還受哪些因素的影響呢?
(猜想與假設)a.可能與鹽酸的濃度有關;b.可能與反應時的溫度有關;c.你的猜想是__________________________________。
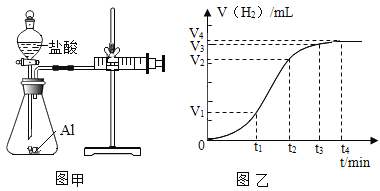
(設計并實驗)小明利用如圖甲所示裝置,用不同質量分數的鹽酸和相同形狀的鋁片進行如下實驗。
(交流討論)請寫出鋁與鹽酸反應的化學方程式:_________________________。
(分析數據)
實驗編號 | 鹽酸的濃度(均取20mL) | 溫度/℃ | 記錄的數據 |
① | 5% | 30 | |
② | 10% | 20 | |
③ | 5% | 20 | |
④ | 10% | 30 |
實驗中記錄的數據可能:_______________________;對比實驗②③可知____對金屬與酸反應的速率有影響。
(拓展延伸1)
小明進行鋁與稀鹽酸反應時,試管外壁發燙,并測得實驗過程中生成氫氣的體積隨時間變化的曲線如圖乙所示,根據曲線歸納鋁與稀鹽酸反應速率的變化規律:_____________。
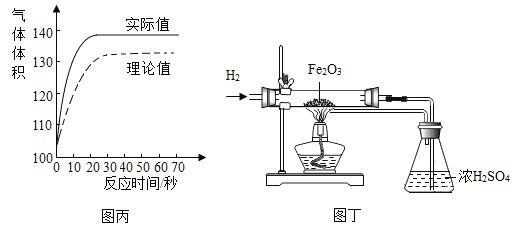
(拓展延伸2 )圖丙為測得的室溫下足量的鋁片與20ml 10%的稀鹽酸反應產生氫氣的量與時間關系曲線,發現實驗測得的實際值比通過計算得到的理論值偏大,請分析可能的原因(至少答兩點)。①__________________,②________________________。
(拓展延伸3 )利用鋁與鹽酸產生的氫氣來做下列實驗,稱取5.2g氧化鐵樣品,放入重48.48g的玻璃管中,按圖丁裝置連接,完全反應后,冷卻至室溫,稱得玻璃管和固體的總質量為52.24g,計算氧化鐵樣品中氧化鐵的質量分數____________。
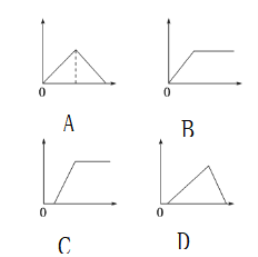
(拓展延伸4)已知氫氧化鈉溶液與氫氧化鋁反應,生成偏鋁酸鈉溶液。在鋁與過量鹽酸反應后的溶液中逐滴加入氫氧化鈉溶液過程中現象為____(下列圖像中,縱坐標為沉淀質量,橫坐標為氫氧化鈉溶液質量 )
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】用化學符號填空:
(1)2個氫原子_____;
(2)3個氮分子_____;
(3)4個碳酸根離子_____;
(4)氧化鎂中鎂元素的化合價為正二價_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在燃燒正旺的炭火盆上,不小心灑上幾滴水,會看到有火苗竄起。這是什么氣體在燃燒?小軍、小虎、小明和小梅組成的合作學習小組對此問題展開了探究。
(組內交流,形成共識)火焰是氣體物質燃燒產生的現象,既然有火苗,水與熾熱的碳反應肯定產生了可燃性氣體,同時應該還有未反應的水蒸氣。
(提出猜想)小軍:可能含有CO;
小梅:可能含有H2;
小明:也可能是CO和H2的混合物;
小虎:不排除有非可燃性氣體生成,有可能還有少量的CO2。
(查閱資料)
無水硫酸銅遇水由白色變為藍色。
(設計實驗)合作學習小組成員設計了如下實驗裝置圖,并進行了實驗。
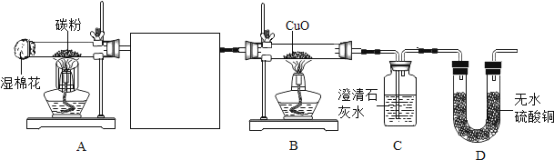
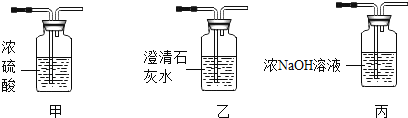
(1)請將上圖甲、乙、丙裝置按一定順序連接后放入上圖方框中,正確的連接順序是_____。
(2)已知試管內棉花不參與反應,它的作用是制造水蒸氣。裝置丙的作用是_____。裝置甲的作用是_____。
(3)實驗中觀察到裝置乙、C中澄清石灰水均變渾濁,B中黑色粉末變紅,D中無水硫酸銅由白色變為藍色。寫出乙中變化的化學方程式_____。
(討論交流)
(4)小軍認為根據上述現象不足以說明產生的氣體中一定存在H2.小梅認為只需將上述裝置稍作改進,就可證明產生的氣體中一定含有H2.小梅的改進是_____。
(5)小明認為該實驗經上述改進后,還存在一個明顯的缺陷,該缺陷是_____。
(實驗結論)熾熱的炭和水蒸氣反應有H2、CO和CO2生成。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】金屬鎂可與熱水反應生成氫氧化鎂和氫氣,所得溶液呈堿性,可使酚酞溶液顯紅色。某同學將鎂條放在水中煮沸,趁熱取出部分溶液,滴加酚酞溶液,變為紅色,放置在空氣中一段時間后,發現溶液的紅色褪去了。
(1)鎂與熱水反應的化學方程式是_______。
(2)查閱資料:溶液紅色褪去的原因是溶液堿性減弱。
(提出問題)導致溶液堿性減弱的原因是什么?
(假設與分析)
假設1:可能是氫氧化鎂與N2或O2發生了反應。
假設2:可能是溶液吸收了空氣中的二氧化碳。
假設3:可能是氫氧化鎂的溶解度隨溫度的降低而_____。
由堿的性質可知,假設1不成立。
(實驗探究)
實驗操作 | 實驗現象 | 結論 |
1.取上述紅色溶液,保持溫度不變,在空氣中放置一段時間,觀察現象。 | _______ | 假設2成立 |
2.取上述紅色溶液,_______觀察現象。 | 紅色褪去 | 假設3成立 |
(拓展延伸)
(3)將一小塊金屬鈉投入硫酸銅溶液時,產生藍色沉淀。請解釋其原因:_________。
(4)除上述金屬外,根據金屬活動性順序,預測_____也能跟硫酸銅溶液反應產生上述現象(舉一例即可)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】氣體的實驗室制取是學生必備的基本實驗技能,某化學興趣小組在實驗室制備并收集CO2。
(1)選用藥品:按表藥品進行實驗,取等質量的大理石加入足量酸中(雜質不與酸反應),產生CO2體積時間變化曲線如下所示:

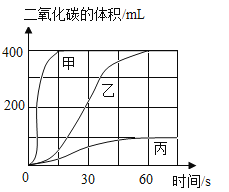
圖中甲對應實驗__________(填“Ⅰ”"Ⅱ”或“Ⅲ"),確定用乙對應的藥品制備并收集CO2,化學方程式為_____________________________,不選用丙對應的藥品的原因____________。
(2)圖中d儀器的名稱是____________,用圖中儀器組裝一套能隨開隨用,隨關隨停約發生裝置,應選用__________
(填字母),該裝置還可用于實驗室制取__________。
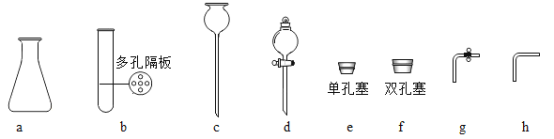
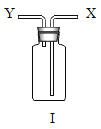
(3)收集并檢驗CO2;
用上圖中的I所示裝置收集CO2時,氣體應從______(填“X"或“Y")端通入;若上圖中的I所示裝置除去CO2中HCl雜質,I中裝的試劑是_______________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某班同學做驗證鐵、銅、銀的金屬活動性順序的實驗,用到的藥品有鐵絲、銅絲、銀絲、稀硫酸和硫酸銅溶液,實驗結束后,化學興趣小組的同學欲對該實驗的廢液進行探究,請你一起參與。
(提出問題)廢液中含有什么物質?
(交流表達)
(1)小明通過觀察,認為廢液中一定含有硫酸銅,他觀察到的現象是_____。
(2)小紅通過分析,認為廢液中一定含有硫酸亞鐵,她的依據是:_____。請寫出鐵絲跟硫酸銅反應的化學方程式:_____。
(作出猜想)小華認為廢液中還可能含有硫酸。
(實驗驗證)
(1)小華測得廢液的pH小于7。
(2)小明取少量廢液,向其中滴加氫氧化鈉溶液,也得到了相同的結論,小明的實驗現象是_____。通過分析與實驗,向同學們得出廢液中含有硫酸亞鐵、硫酸銅和硫酸。
(拓展應用)
(1)請寫出硫酸銅與氫氧化鈉溶液反應的化學方程式:_____。該反應的實驗現象為_____。
(2)取少量廢液,加入過量的鐵屑,反應完全后,過濾,濾渣中物質為_____,濾液中溶質為硫酸亞鐵。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】A、B、C、D、E是九年級化學中常見的五種物質。已知C是人體胃液中可以幫助消化的物質,D是大理石的主要成分,其相互反應及轉化關系如下圖所示,“一”表示相連的兩物質之間能發生反應,“→”表示一種物質能轉化為另一種物質,部分反應條件、反應物、生成物已略去。

(1)寫出物質E的化學式_________。
(2)B轉化為A的反應化學方程式:_________;C與D反應的化學方程式:_______
(3)圖中涉及的反應中,屬于復分解反應的有_______個。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com