
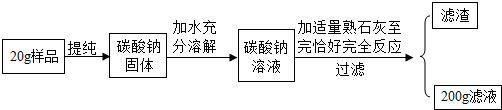
分析 (1)碳酸鈉的質量=樣品的質量×含碳酸鈉的質量分數;
(2)根據化學方程式結合碳酸鈉的質量求解氫氧化鈉的質量,進一步計算所得濾液中氫氧化鈉的質量分數;
(3)根據溶液稀釋前后溶質質量不變解答.
解答 解:(1)碳酸鈉的質量為20g×53%=10.6g;
(2)設反應生成氫氧化鈉的質量為x;
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
10.6g x
$\frac{106}{10.6g}=\frac{80}{x}$
解得x=8g
氫氧化鈉的質量分數=$\frac{8g}{200g}$×100%=4%
答:反應后所得濾液中氫氧化鈉的質量分數為4%.
(3)設需蒸發水y
200g×4%=(200g-y)×10%
y=120g
故答案為:
(1)10.6;
(2)4%;
(3)120
點評 本題重點考查了化學方程式的有關計算方法、步驟和格式;它是一道很傳統的根據化學方程式計算的題目.解答時,只要細心地分析審題后,按照有關化學方程式的計算步驟和格式,進行計算即可.


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:填空題
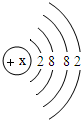 ,該元素的原子序數為20,原子核外有4個電子層;該元素屬于金屬(填“金屬”和“非金屬”)元素,該元素原子失去最外層電子所形成的離子為Ca2+(用離子符號表示).
,該元素的原子序數為20,原子核外有4個電子層;該元素屬于金屬(填“金屬”和“非金屬”)元素,該元素原子失去最外層電子所形成的離子為Ca2+(用離子符號表示).查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
| 實驗操作 | 實驗現象 | 實驗結論 |
| ①取少量固體放于試管中,加入蒸餾水充分攪拌 | 用手觸摸試管,試管外壁發燙 | 固體中一定含有氧化鈣 |
| ②另取少量固體放于試管中,滴加足量稀鹽酸 | 固體逐漸消失,有大量無色氣體產生,得到淺綠色溶液 | 固體中一定含有鐵,一定不含Fe2O3 |
| ③將步驟②中產生的氣體通入澄清的石灰水中 | 澄清石灰水變渾濁 | 固體中一定含有CaCO3 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | Ca2+、Cu2+、NO3-、Cl- | B. | Na+、Mg2+、SO42-、Cl-、 | ||
| C. | Na+、K+、CO32-、SO42- | D. | Na+、Ba2+、Cl-、NO3- |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題

| A. | 甲是有機物 | B. | 該反應有元素化合價的改變 | ||
| C. | 反應的本質是原子重新組合的過程 | D. | 參加反應的甲和乙的質量比是1;3 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 氧化物含氧元素,所以含氧元素的物質一定是氧化物 | |
| B. | 蠟燭燃燒生成二氧化碳和水,所以蠟燭組成元素中一定含有碳元素和氫元素 | |
| C. | 物質的燃燒需同時滿足三個條件,所以滅火一定要同時破壞這三個條件 | |
| D. | 堿的溶液pH值大于7,所以pH值大于7的溶液一定是堿的溶液 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com