
在一個密閉容器中放入W、G、H、P四種物質,在一定條件下發生化學反應,一段時間后,測得有關數據如下表:
| 物質 | W | G | H | P |
| 反應前質量/g | 18 | 1 | 2 | 32 |
| 反應后質量/g | 待測 | 26 | 2 | 12 |
對該反應的認識正確的是( )
|
| A. | W待測值是13 | B. | 該反應是分解反應 |
|
| C. | P是生成物 | D. | 物質H是該反應的催化劑 |
| 質量守恒定律及其應用.. | |
| 專題: | 化學用語和質量守恒定律. |
| 分析: | 根據質量守恒定律可知,參加反應的各物質質量總和等于反應后生成的各物質的質量總和.化學反應后,質量增加的物質是生成物,質量減少的物質是反應物.利用這一性質進行判斷. |
| 解答: | 解:由表中信息可知,P物質的質量減少為反應物,參加反應的質量是20克;G物質的質量增加為生成物,生成的質量是25克;H物質的質量不變故H物質不參與反應.根據質量守恒定律可知,W是反應物,參加反應的質量是5克. A、反應后物質W的質量為:18g﹣5g=13g.故A正確; B、反應物是兩種,生成物是一種,屬于化合反應,故B錯誤; C、P物質的質量減少故為反應物.故C錯誤; D、物質H的質量在反應前后不變,可能是該反應的催化劑,故D錯誤. 故選A. |
| 點評: | 在化學反應中遵循質量守恒定律,參加反應的物質的質量等于反應后生成的物質的質量. |


 金鑰匙試卷系列答案
金鑰匙試卷系列答案科目:初中化學 來源: 題型:
某化學興趣小組在學習氧氣的制法后進行一系列探究活動。
探究1.
利用如圖實驗裝置制取氧氣。
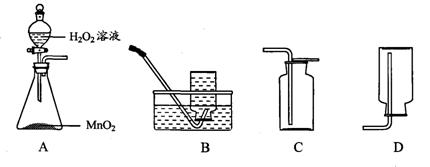
(1)寫出用A裝置制取氧氣的化學方程式 ▲ 。
探究2.
(2)小組對過氧化氫分解時影響反應速率的部分因素作出探究,并測得相關實驗數據。如表:
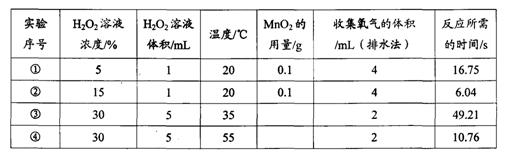
從實驗③和④對比可知,化學反應速率與 ▲ 有關。通過實驗 ▲ 與實驗 ▲ (填實驗序號)對比可知,化學反應速率與反應物的濃度有關。若用一定量15%的過氧化氫溶液制氧氣,為了減小反應速率,加適量水稀釋,產生氧氣的總質量 ▲ 。(選填“減小”或“不變”或“增大”)。
探究3.
小組中小童同學取15%的H2O2溶液5mL于試管中,加熱后,觀察到溶液中產生較多氣泡,他直接將帶火星的木條伸入試管中,木條卻沒有復燃,直至溶液沸騰,也未見木條復燃。小組一起反復實驗討論并通過查找資料找到了木條不能復燃的原因。
(3)有關小童在實驗中帶火星的木條沒有復燃,下列說法中正確的有 ▲ 。
A.實驗所用的過氧化氫溶液的濃度太小。
B.加熱過氧化氫能分解,但反應速率較慢,試管中氧氣含量較少。
C.加熱過氧化氫溶液的同時,溶液中的水蒸氣隨氧氣一起逸出,環境濕度較大,木條不能復燃。
D.小童采用排水法去收集產生的氣體,再用帶火星木條檢驗,木條能復燃。
查看答案和解析>>
科目:初中化學 來源: 題型:
二甲醚(C2H6O)作為一種新能源,有關說法正確的是( )
|
| A. | 二甲醚的相對分子質量為48 |
|
| B. | 二甲醚屬于氧化物 |
|
| C. | 二甲醚由2個碳原子、6個氫原子和1個氧原子構成 |
|
| D. | 二甲醚中碳元素與氫元素的質量比為4:1 |
查看答案和解析>>
科目:初中化學 來源: 題型:
請認真回憶物質與其構成粒子之間的關系,回答下列問題:
(1)金屬鐵是由 (填“原子”、“分子”或“離子”,下同)構成的,氯化鉀是由 構成的,二氧化碳是由 構成的.
(2)原子得到或失去電子后形成離子.某粒子的結構示意圖為
①當a= 時,該粒子是原子,該原子位于元素周期表中第 周期.
②當a=8時,該粒子是 (填“原子”、“陽離子”或“陰離子”).
查看答案和解析>>
科目:初中化學 來源: 題型:
食品中加入抗氧化劑可防止食品腐敗,BHT(化學式C13H30O)是一種抗氧化劑,該物質的相對分子質量是 ,C、H、O的原子個數比是 ,碳元素的質量分數是 (精確至0.1%).
查看答案和解析>>
科目:初中化學 來源: 題型:
通過一階段的學習,我們懂得了一些化學知識,請按要求填空:
(1)供給人類呼吸的氣體是 ;
(2)氫單質 H2 ;3個鎂離子 ;﹣2價的硫元素 ;氯化鈉 ;硝酸銅 ;
(3)最理想的清潔燃料是 ,燃燒產生 色火焰.
查看答案和解析>>
科目:初中化學 來源: 題型:
已知A、B為兩種黑色粉末,D為紅色單質。A、B、C、D、E五種物質之間的轉化關系如圖10所示。
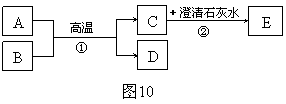 |
請回答:
(1)C的化學式為 ________ ;
(2)A中金屬元素的化合價是______ __;
__;
(3)反應①的化學方程式為 ________;
該反應的基本類型是 _____ ___。
___。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com