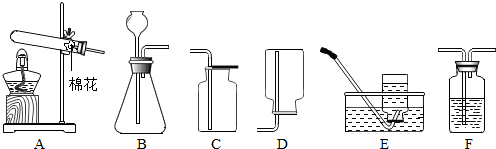
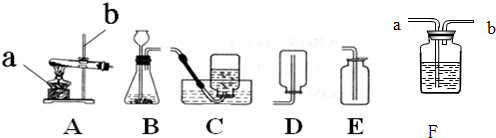
解:(1)依據實驗室常用儀器的認識解決此題:①長頸漏斗;②集氣瓶;
(2)錯誤:①A圖中,給試管中的固體物質加熱時,試管口向上傾斜了,應該略向下傾斜;②E圖中,用向上排空氣法收集氣體時,導氣管伸入過短,應伸入集氣瓶的底部,才能盡可能排凈原有空氣.
(3)小明在實驗室中用氯化鉀和二氧化錳制取氧氣,他選擇上述裝置中的A和E或F或D;分別寫出小明、小紅制取氧氣的化學反應方程式:2KClO
3
2KCl+3O
2↑,2H
2O
2
2H
2O+O
2↑;
(4)實驗室用B裝置制取二氧化碳的化學方程式:CaCO
3+2HCl═2CaCl
2+H
2O+CO
2↑;
(5)觀察的現象是:燒杯內下面蠟燭先熄滅,上面蠟燭后熄滅;該實驗能說明二氧化碳既不燃燒也不能支持燃燒且密度比空氣大的性質;
(6)實驗室選擇氣體發生裝置應考慮反應物的狀態和反應條件;
(7)實驗室常用加熱無水醋酸鈉和堿石灰兩種固體物質的混合物來制取甲烷.可選用以上裝置中的A作為實驗室制取甲烷的發生裝置.如果用F裝置收集甲烷,氣體應從b端管口通入.
(8)解:設高錳酸鉀的質量為X
2KMnO
4
K
2MnO
4+MnO
2+O
2↑
316 32
X 1.6g
316:32=X:1.6g
X=15.8g
答:高錳酸鉀的質量為15.8g.
故答案為:
(1)①鐵架臺;②集氣瓶;
(2)①A圖中,給試管中的固體物質加熱時,試管口向上傾斜了,應該略向下傾斜;
②D圖中,用向上排空氣法收集氣體時,導氣管伸入過短,應伸入集氣瓶的底部.
(3)E或F或D,2KClO
3
2KCl+3O
2↑,2H
2O
2
2H
2O+O
2↑,可以隨時控制反應的進行,隨開隨停;不需加熱,操作簡便;
(4)CaCO
3+2HCl═2CaCl
2+H
2O+CO
2↑;
(5)下層的蠟燭先熄滅,上層的后熄滅,密度比空氣大,不能燃燒也不能支持燃燒;
(6)反應物的狀態,反應條件;
(7)A b;
(8)解:設高錳酸鉀的質量為X
2KMnO
4
K
2MnO
4+MnO
2+O
2↑
316 32
X 1.6g
316:32=X:1.6g
X=15.8g
答:高錳酸鉀的質量為15.8g.
分析:(1)依據實驗室常用儀器的認識解決此題;
(2)①加熱固體時:試管口要向下傾斜,防止有水生成,倒流炸裂試管;②導氣管伸入過短,不能排凈原有空氣;
(3)①用氯酸鉀和另一種固體制取氧氣“固體+固體”,且需要加熱,且氧氣難溶于水,密度比空氣的大,故選用A裝置與E或F或G;②選用C裝置作為氧氣的發生裝置,不需要加熱,則為用過氧化氫溶液和二氧化錳制取氧氣;B裝置一個突出優點可以隨時控制反應的進行;
(4)寫出實驗室用B裝置制取二氧化碳的化學方程式;
(5)根據二氧化碳既不燃燒也不能支持燃燒且密度比空氣大的性質解答;
(6)實驗室選擇氣體發生裝置應考慮反應物的狀態和反應條件;
(7)因為實驗室常用加熱無水醋酸鈉和堿石灰兩種固體物質的混合物來制取甲烷,應選擇固+固加熱型發生裝置;根據F裝置的特點選擇收集甲烷的方法.
(8)根據實驗室用加熱高錳酸鉀的方法制取氧氣的化學方程式進行計算,已知生成的氧氣的質量,求得反應的高錳酸鉀的質量.
點評:學會比較用碳酸鈣與鹽酸制取二氧化碳、用氯酸鉀制取氧氣和用過氧化氫溶液和二氧化錳制取氧氣的區別聯系;掌握制取氧氣和二氧化碳的反應原理、制法及操作步驟和注意點;掌握二氧化碳的性質及有關化學方程式的計算;此題綜合性很強.



 2KCl+3O2↑,2H2O2
2KCl+3O2↑,2H2O2 2H2O+O2↑;
2H2O+O2↑; K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑  2KCl+3O2↑,2H2O2
2KCl+3O2↑,2H2O2 2H2O+O2↑,可以隨時控制反應的進行,隨開隨停;不需加熱,操作簡便;
2H2O+O2↑,可以隨時控制反應的進行,隨開隨停;不需加熱,操作簡便; K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑ 

 通城學典默寫能手系列答案
通城學典默寫能手系列答案 金牌教輔培優優選卷期末沖刺100分系列答案
金牌教輔培優優選卷期末沖刺100分系列答案