
分析 氫氧化鈉和二氧化碳反應生成碳酸鈉和水,碳酸鈉和稀硫酸反應生成硫酸鈉、水和二氧化碳,氫氧化鈉和稀硫酸反應生成硫酸鈉和水,反應前后的質量差即為反應生成二氧化碳的質量,根據二氧化碳質量可以計算碳酸鈉質量,進一步可以計算該樣品中Na2CO3的質量分數.
解答 解:(1)設碳酸鈉質量為x,
反應生成二氧化碳質量為:13.5g+75g-86.3g=2.2g,
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑,
106 44
x 2.2g
$\frac{106}{x}$=$\frac{44}{2.2g}$,
x=5.3g,
該樣品中Na2CO3的質量分數為:$\frac{5.3g}{13.5g}$×100%=39.3%,
答:該樣品中Na2CO3的質量分數為39.3%.
(2)氫氧化鈉和二氧化碳、稀硫酸、碳酸鈉和稀硫酸反應的化學方程式為:2NaOH+CO2═Na2CO3+H2O,2NaOH+H2SO4═Na2SO4+2H2O,Na2CO3+H2SO4═Na2SO4+H2O+CO2↑,由反應的化學方程式可知,恰好完全反應時消耗硫酸的量相等.
故填:相等.
點評 差量法在計算中的應用很廣泛,解答的關鍵是要分析出物質的質量差與要求的未知數之間的關系,再根據具體的數據求解.


科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
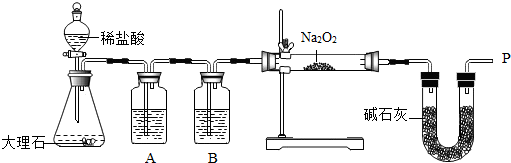
| 實驗操作 | 實驗現象 |
| Ⅰ.打開分液漏斗旋塞,向錐形瓶中注入足量稀鹽酸后關閉;一段時間后在導管口P處用帶火星的木條檢驗導出的氣體 | 錐形瓶內產生大量氣泡 |
| Ⅱ.觀察到玻璃管內固體變為白色后,再次測定玻璃管內固體質量;測定固體質量完畢后將固體溶于盛有適量水的燒杯中 | 燒杯中無明顯現象 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 該反應為置換反應 | |
| B. | Na2O2中氧元素的化合價為-2價 | |
| C. | X的相對分子質量為116 | |
| D. | 利用該反應可以維持艇內空氣成分的相對穩定 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | NaCl溶液 | B. | 稀硫酸 | C. | Na2CO3溶液 | D. | AgNO3溶液 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
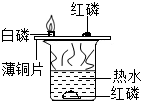 如圖所示,某同學在500毫升的燒杯中注入300毫升80℃的熱水,并投入少量紅磷.在燒杯上蓋上一片薄銅片,銅片上一端放上一小堆干燥的紅磷,另一端放上一小塊已用濾紙吸去表面上水分的白磷.
如圖所示,某同學在500毫升的燒杯中注入300毫升80℃的熱水,并投入少量紅磷.在燒杯上蓋上一片薄銅片,銅片上一端放上一小堆干燥的紅磷,另一端放上一小塊已用濾紙吸去表面上水分的白磷.查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com