
溶液的應用非常廣泛。K2CO3和KNO3在不同溫度時的溶解度及其溶解度曲線如下: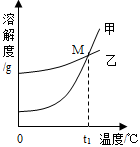
(1)硝酸鉀溶液中的溶劑是_______________。
(2)圖中能表示KNO3溶解度曲線的是__________(填“甲”或“乙”)。
(3)溶解度曲線上M點的含義是___________。
(4)現有200g溶質質量分數為10%的碳酸鉀溶液,若使溶液的溶質質量分數增加一倍,應該蒸發掉 g水。
(5)40℃時,向兩個分別盛有相同質量的硝酸鉀和碳酸鉀的燒杯中,各加入100g水,充分溶解后,恢復至40℃,其結果如右圖所示。下列有關說法中,正確的是_________(填字母序號)。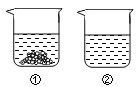
| A.燒杯②中溶液一定是不飽和溶液 |
| B.若使燒杯①中固體全部溶解,溶液中溶質質量分數一定增大 |
| C.將燒杯②中溶液降溫至20℃時,溶液中溶質質量分數可能增大 |
| D.若將燒杯①中的溶液變為不飽和溶液,溶液中溶質質量分數可能增大 |
(1)水 (2)甲
(3)t1°C時,碳酸鉀和硝酸鉀的溶解度相等。
(4)100 (5)D
解析試題分析:(1)硝酸鉀溶液就是硝酸鉀的水溶液,故其中的溶劑是水。
(2)根據題給的溶解度表可知,在20℃——60℃時硝酸鉀的溶解度小于碳酸鉀,在80℃時硝酸鉀的溶解度小大于碳酸鉀,再結合圖中的兩條溶解度曲線可知,甲表示的是硝酸鉀的溶解度曲線。
(3)根據溶解度曲線圖可知,曲線上的交點的含義表示:此溫度下,兩種物質的溶解度相等,所以溶解度曲線上M點的含義是t1℃時,KNO3和K2CO3的溶解度相等。
(4)由于溶液蒸發溶劑前后,溶質的質量不變,據此分析。設應蒸發掉水的質量為x,則200g×10%=(200g-x)×20%,解得x=100g。
(5)根據題意,結合溶解度曲線分析。
A、由于40℃時硝酸鉀的溶解度較小,故有不溶物的是硝酸鉀溶液,且已達到飽和;則全部溶解的是碳酸鉀溶液,但全部溶解可能剛好飽和,也可能不飽和,故錯誤;
B、若使燒杯①中固體全部溶解,可通過加入溶劑來實現,則溶液中溶質質量分數不一定增大,錯誤;
C、由于碳酸鉀的溶解度隨溫度的升高而增大,故將燒杯②中溶液降溫至20℃時,有可能有溶質析出,也有可能沒有,所以溶液中溶質質量分數不可能增大,錯誤;
D、由于硝酸鉀的溶解度隨溫度的升高而增大,所以通過升高溫度,能將燒杯①中的溶液變為不飽和溶液,則溶液中溶質質量分數可能增大,正確。故選D
考點:溶液的組成及溶質、溶劑的關系,固體溶解度曲線及其作用,飽和溶液和不飽和溶液,飽和溶液和不飽和溶液相互轉變的方法,溶質質量分數的計算
點評:本題主要考查了固體溶解度曲線所表示的意義,及根據固體溶解度曲線來解決相關問題,注重培養學生的分析問題、解決問題的能力,解題的關鍵是要熟記和理解固體溶解度曲線及其應用,以及溶質質量分數的有關計算。


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:

| 溫度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
查看答案和解析>>
科目:初中化學 來源: 題型:
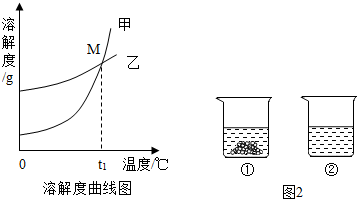
 生產和生活中溶液的應用非常廣泛.K2CO3和KNO3在不同溫度時的溶解度及其溶解度曲線如圖.
生產和生活中溶液的應用非常廣泛.K2CO3和KNO3在不同溫度時的溶解度及其溶解度曲線如圖.| 溫度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3 | 110 | 114科網] | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
查看答案和解析>>
科目:初中化學 來源: 題型:
| 溫度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
查看答案和解析>>
科目:初中化學 來源: 題型:
| 溫度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |

查看答案和解析>>
科目:初中化學 來源: 題型:
 (2013?高郵市二模)溶液的應用非常廣泛.
(2013?高郵市二模)溶液的應用非常廣泛.| 溫度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com