
我國早在春秋戰國時期,就開始生產和使用鐵器。某化學小組到鋼鐵廠做社會調查,將不同質量的生鐵樣品(假定其中只含鐵和碳兩種單質)分別放入5只燒杯中,各加入189.2 g質量分數相同的稀硫酸進行實驗,實驗數據見下表:
| 燒杯① | 燒杯② | 燒杯③ | 燒杯④ | 燒杯⑤ |
加入生鐵樣品 的質量/g | 3.0 | 6.0 | 9.0 | 12.4 | 14.0 |
充分反應后 生成氣體 的質量/g | 0.1 | M | 0.3 | 0.4 | 0.4 |
試計算:
(1)表中M的值為________。
(2)燒杯④中完全反應后,所得溶液中溶質的質量是多少?(寫出計算過程)
(1)0.2?? (2)30.4 g(計算過程見解析)
【解析】本題以某化學小組到鋼鐵廠做社會調查,將不同質量的生鐵樣品與稀硫酸反應的數據為主題,考查化學方程式的計算。解題的關鍵有:(1)首先要推斷出M的數值。比較燒杯①和燒杯③中的生鐵樣品及產生的氣體可以知道,每3.0 g生鐵樣品與足量稀硫酸反應后能生成0.1 g氫氣,所以可以判斷M的值為0.2;(2)分析表中數據,明確哪組實驗中鐵樣品和稀硫酸完全反應。比較燒杯③和燒杯④中數據可以知道,生鐵的質量增加12.4 g-9.0 g=3.4 g,但是氣體的質量只增加了0.1 g,結合(1)的分析可以判斷稀硫酸已完全反應。(3)知道189.2 g稀硫酸可以消耗生鐵的質量為12.0 g,此時,溶液中的溶質為硫酸亞鐵,據此結合化學方程式來完成解答。
解:設生成硫酸亞鐵的質量為y。
Fe+H2SO4=FeSO4+H2↑
???????? 152??? 2
????????? y??? 0.4 g
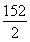 =
= 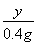
y= 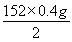 =30.4 g
=30.4 g
答:所得FeSO4溶液中溶質的質量為30.4 g


 小學課時作業全通練案系列答案
小學課時作業全通練案系列答案 金版課堂課時訓練系列答案
金版課堂課時訓練系列答案科目:初中化學 來源: 題型:
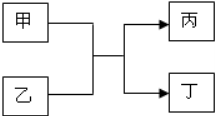 甲、乙、丙、丁是初中化學的常見物質,它們有如圖的轉化關系:
甲、乙、丙、丁是初中化學的常見物質,它們有如圖的轉化關系:查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
| ||
| ||
查看答案和解析>>
科目:初中化學 來源: 題型:
| ||
| ||
| ||
| ||

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com