
【題目】氨氣可用于處理硝酸工廠排放的一氧化氮氣體,該反應前后微粒種類如下圖所示。下列說法正確的是

A.該反應不符合質量守恒定律
B.反應前后分子和原子的種類都不變
C.參加反應的X 和Y 的質量比為 30:17
D.反應生成的 Z 和W 的分子個數比為 5:6
【答案】D
【解析】
根據反應的微觀示意圖,分析反應物、生成物,寫出化學式、方程式,根據其意義分析判斷有關的問題;根據微粒的變化,分析分子、原子的變化等。
由反應的微觀示意圖可知,該反應是一氧化氮和氨氣在催化劑作用下反應生成了氮氣和水,反應的方程式是: 。
。
A、該反應有新物質生成,是化學變化,而一切化學反應都遵從質量守恒定律,故A錯誤;
B、根據化學變化的特征可知:在化學反應前后,分子種類一定改變而原子的種類保持不變,故B錯誤;
C、由方程式可知,該反應中X、Y兩種物質的質量比為(30×6):(17×4)=45:17,故C錯誤;
D、由方程式可知,Z和W兩物質的分子個數比為5:6,故D正確。
故選D。


科目:初中化學 來源: 題型:
【題目】燃燒是生活中常見的現象。
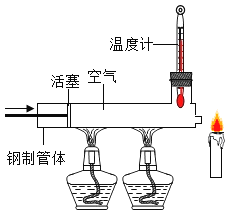
(1)已知石蠟的著火點約為190℃,蠟燭的火焰由氣態石蠟燃燒形成。如圖所示,在溫度計讀數為280℃以上時,快速推動活塞,觀察到蠟燭立即熄滅。蠟燭熄滅的主要原因是什么?_____
(2)油庫、面粉加工廠、加油站等場所都要嚴禁煙火,其原因是什么?_____
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】我國化學家侯德榜發明了聯合制堿法,其生產純堿的產品和副產品氯化銨的工藝流程如圖所示:

(1)NH3溶于水得到氨水,將無色酚酞溶液滴入氨水中,溶液呈 色.
(2)寫出反應I的化學方程式 ;該反應的基本類型為 .
(3)操作a的過程是蒸發濃縮、 、過濾.
(4)上述工藝流程中可循環利用的物質是 .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】四種物質在一定的條件下充分混合反應,測得反應前后各物質的質量分數如圖所示。則下列有關說法中不正確的是
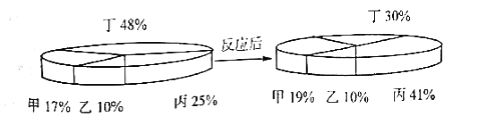
A. 生成的甲、丙兩物質的質量比例為1:8 B. 乙一定是這個反應的催化劑
C. 甲可能是單質 D. 參加反應的丁的質量一定等于生成甲和丙的質量之和
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】從鹽湖中提取的某種礦物主要含有氯化鉀,還有少量硫酸鎂、氯化鈣及不溶性雜質SiO2,從該礦物中提取氯化鉀的流程如下圖。
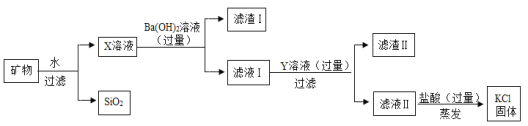
回答下列問題 :
(1)濾渣Ⅰ的主要成分是____________;
(2)Y溶液中溶質的化學式為____________;
(3)向濾液Ⅱ中加入過量鹽酸的目的是____________;
(4)蒸發溶液得到氯化鉀固體的過程中,要用玻璃棒不斷攪拌,目的是____________ 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】以天然氣(含少量 H2S 氣體)為原料可獲得工業合成氨所需的 N2 和 H2,其轉化步驟如下:
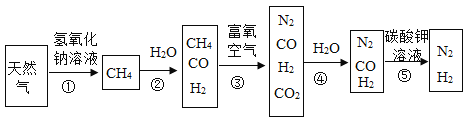
(1)天然氣屬于____燃料。合成氨的反應方程式為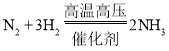 ,該反應屬于_________(填基本反應類型)。氨氣(NH3)常用于制備__________(填“氮”、“磷”或“鉀”)肥。
,該反應屬于_________(填基本反應類型)。氨氣(NH3)常用于制備__________(填“氮”、“磷”或“鉀”)肥。
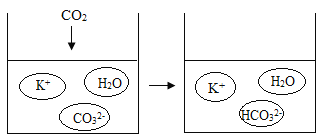
(2)步驟⑤中所涉化學反應前后主要微粒種類變化如圖所示。試寫出該反應的化學方程式:_______。
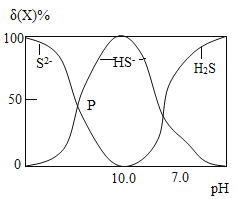
(3)步驟①中所用NaOH 溶液可吸收天然氣中的H2S 氣體并與之發生反應。常溫下隨著 H2S不斷被吸收,NaOH 溶液的pH逐漸減小,溶液中含硫粒子(S2-、HS-、H2S)的分布δ(X)如圖所示。
注:已知H2S氣體溶于水后可解離出H+、HS-和 S2-。
δ(X)=![]()
①溶液的 pH=7 時,溶液呈________(填“酸性”、“堿性”或“中性”)。P 點對應的溶液中溶質主要為NaHS 和________,溶液中 S2-的個數_________(填“大于”、“等于”或“小于”)HS-的個數。
②當溶液的 pH=10 時,NaOH 與H2S 反應的化學方程式為____________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】山西省是煤炭大省,近幾年正積極推動綠色低碳高效開發利用煤炭。
(1)煤炭綜合利用的方法之一是煤的氣化。 煤的氣化就是把煤轉化為可燃性氣體的過程。 在高溫下煤和水蒸氣作用得到 CO、H2、CH4 等氣體,生成的氣體可作為燃料或化工原料氣。 請任寫出其中一種 氣體化合物燃燒的化學反應方程式:__________。
(2)下列活動中,通過化學反應提供能量的是______________。
A 發射航天飛機 B
發射航天飛機 B 水車汲水灌溉
水車汲水灌溉
C 太陽能供熱 D
太陽能供熱 D 風力發電
風力發電
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】現有一包含有雜質的BaCl2固體樣品(雜質不溶于水),為了研究樣品的組成,進行了如下試驗。請回答下列問題:
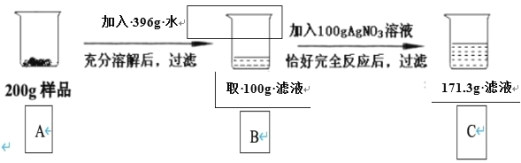
(1)實驗發生反應的化學方程式為_____。
(2)列出求解硝酸銀溶液中溶質質量(x)的比例式_____。
(3)200g固體樣品加水充分溶解后,所得溶液的溶質質量分數為_____。
(4)在C燒杯加入多少克水使其中濾液的溶質質量分數為10%_____。
(5)向燒杯中加入硝酸銀溶液的過程中,用數據說明濾液中溶質的變化情況是_____。
(6)樣品中BaCl2的純度為_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】試劑A、B、C是Na2CO3溶液、稀鹽酸、Ca(OH) 2溶液中的一種。某同學進行如圖所示的實驗,觀察到試管①中無明顯現象,試管②中溶液變渾濁。實驗結束后,該同學把試管①、②中的物質全部倒入燒杯中,發現溶液變澄清,并有氣泡冒出。
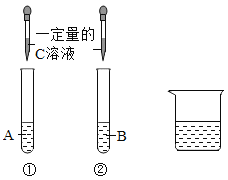
(1)A是_____________,B的溶質是_____________(填俗名)。
(2)寫出試管A中的反應化學方程式:_____________。
(3)寫出燒杯中溶液變澄清的反應化學方程式:_____________。
(4)燒杯中所得溶液的溶質可能是_____________(填序號)。
a NaCl、 Na2CO3
b NaCl、CaCl2、HCl
c NaCl、CaCl2
d NaCl、CaCl2、Na2CO3
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com