同學們對課本上“活動性較強的金屬一般可以將位于其后面的金屬從它們的鹽溶液中置換出來”以及“支持燃燒的氣體一般是氧氣”這兩句話產生了質疑.在老師的幫助下,用金屬鈉來探究下列問題:
[提出問題]1.金屬鈉能否置換出硫酸銅溶液中的銅?2.金屬鈉能否在其他氣體(如:CO
2)中燃燒?
[查閱資料]金屬Na性質活潑,常溫下,它極易與氧氣反應生成白色固體氧化鈉,氧化鈉溶于水生成氫氧化鈉.金屬鈉還可以與水劇烈反應放出氫氣.
[實驗探究]實驗一:①在實驗室中,金屬鈉保存在煤油中;②用鑷子從煤油中取出一小塊金屬鈉,用濾紙吸干表面煤油后投入硫酸銅溶液中,觀察到溶液中出現藍色沉淀,但沒有紅色的物質析出;
③按照步驟②將金屬鈉投入水中,待反應結束后滴加酚酞溶液,發現溶液變紅.
實驗二:將燃燒的鈉迅速伸入盛有CO
2的集氣瓶中,觀察到鈉在CO
2中繼續燃燒,反應后冷卻,瓶內附著黑色顆粒,并粘附著白色物質.
[問題討論](1)金屬鈉保存在煤油中的原因
鈉易與氧氣反應變質
鈉易與氧氣反應變質
.
(2)根據上述資料寫出鈉塊投入水中所發生的反應方程式:
2Na+2H2O═2NaOH+H2↑
2Na+2H2O═2NaOH+H2↑
;鈉投入硫酸銅溶液中總的反應方程式:
2Na+2H2O+CuSO4=H2↑+Cu(OH)2↓+Na2SO4
2Na+2H2O+CuSO4=H2↑+Cu(OH)2↓+Na2SO4
.氫氧化銅受熱分解成氧化銅和水,若將24.0g剩余固體繼續高溫加熱,發現固體質量減少了2.4g后質量不再改變,寫出此過程中可能發生反應的化學方程式:
.
(3)實驗二中生成的黑色顆粒是
C
C
,而白色物質可能是什么呢?
①同學們圍繞白色物質可能是什么產生如下猜想:甲認為白色物質是Na
2O,乙認為是Na
2CO
3,丙認為是Na
2O和Na
2CO
3的混合物,丁認為是NaOH.
我認為認為丁的猜想是錯誤的,理由是
反應物中沒有氫元素
反應物中沒有氫元素
.
②對白色物質是什么進行實驗再探究,方案設計如下:
方案1:取該樣品少量于試管里,加入適量的水,振蕩,過濾,向濾液中加入無色酚酞試液,觀察到溶液變成紅色,結論:白色物質中一定有Na
2O.
方案2:取該樣品少量于試管里,滴加足量稀鹽酸,溶液中有氣泡冒出,結論:白色物質中一定有
碳酸鈉
碳酸鈉
.
方案3:取該樣品少量于試管里,加入適量的水,振蕩,過濾,向濾液中加入過量的
B
B
溶液(供選試劑:A.石灰水B.氯化鈣溶液 C.硫酸銅溶液),出現白色沉淀,然后過濾,再向溶液里滴加無色酚酞試液,無明顯現象出現.則
乙
乙
(在甲、乙、丙中選)的猜想成立.
③評價與反思:大家認為實驗方案1得出的結論不正確,其理由是
碳酸鈉溶液也是堿性的
碳酸鈉溶液也是堿性的
;
實驗室中的金屬鈉著火時,你的滅火方法是
用黃沙掩埋
用黃沙掩埋
.
[拓展應用]小明同學為測定實驗過程中所用的標示質量分數為32%的鹽酸 (圖1)的實際質量分數,他與小組的其他同學用pH測定儀組成實驗裝置(圖2).實驗時先在燒杯中加入20g 40%的氫氧化鈉溶液,再逐滴加人該鹽酸,測定儀打印出加入鹽酸的質量與燒杯中溶液pH的關系圖(圖3).

①發生反應的化學方程式為:
HCl+NaOH=NaCl+H2O
HCl+NaOH=NaCl+H2O
_.
②請以此次測定的結果,可計算出該鹽酸的實際質量分數是
29.2%
29.2%
.
③請分析你的計算結果與標簽標示的質量分數不一致的可能原因:
濃鹽酸具有揮發性,長期放置質量分數減小
濃鹽酸具有揮發性,長期放置質量分數減小
.

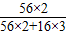 ×100%=70%;
×100%=70%;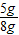 ×100%=62.5%;
×100%=62.5%;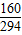 =
=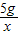
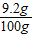 ×100%=9.2%.
×100%=9.2%.

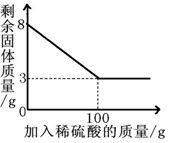
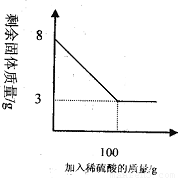
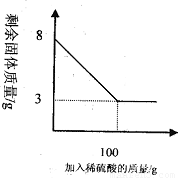
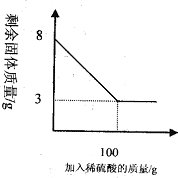 小明同學為測定某種混合物(成分為Fe2O3和C)中Fe2O3含量,稱取8g樣品與足量稀硫酸反應,得到數據如下圖所示.請回答下列問題:
小明同學為測定某種混合物(成分為Fe2O3和C)中Fe2O3含量,稱取8g樣品與足量稀硫酸反應,得到數據如下圖所示.請回答下列問題: