
(6分)小明家購買了一瓶白醋,標簽上注明醋酸的質量分數≥5%。小明想:這瓶白醋中醋酸的含量是否與標簽的標注相符?請你用有關酸堿的知識,定量測定白醋中醋酸的含量。
【實驗原理】
⑴用已知濃度的氫氧化鈉溶液和醋酸反應,反應的化學方程式為:
CH3COOH + NaOH = CH3COONa + H2O
⑵在混合溶液中,當醋酸和氫氧化鈉完全中和時,再增加1滴氫氧化鈉溶液,溶液就呈堿性,而1滴氫氧化鈉溶液約為0.05 ml,對測定結果的影響很小,可忽略不計。
【實驗步驟】
⑴用 取12.0 mL白醋(密度近似為1.0g/ ml),倒入燒杯中,加入20 ml蒸餾水稀釋,再滴入幾滴酚酞試液。
⑵量取45.0 ml溶質質量分數為1.0%的氫氧化鈉溶液(密度近似為1.0 g/ ml),用膠頭滴管取該氫氧化鈉溶液,逐滴地滴加到稀釋后的白醋中,同時不斷地攪拌燒杯中的溶液。滴至恰好完全反應,剩余氫氧化鈉溶液5.0 ml。
【交流反思】⑴在實驗步驟①中,加適量水稀釋白醋,對實驗結果有無影響?為什么?
⑵在實驗步驟②中,小明如何確定醋酸和氫氧化鈉已完全中和?
【數據處理】根據實驗數據,通過計算判斷白醋中醋酸的含量是否與標簽的標注相符?(3分)
【實驗步驟】(1)量筒
【交流反思】(1)沒有影響,因為溶質的質量不變
(2)滴入最后一滴氫氧化鈉溶液時,燒杯中液體由無色變紅色
【數據處理】與標簽的標注相符
解析試題分析:【實驗步驟】(1)量取液體的體積時需要用到量筒
【交流反思】(1)根據酸堿中和反應的實質,我們知道,加入水只是將溶液進行了稀釋,而溶質的質量并沒有發生變化,故沒有影響;
(2) 由于醋酸與氫氧化鈉反應沒有明顯現象,所以可滴入幾滴酚酞試液作指示劑,酚酞試液遇酸不變色,遇堿變紅色,遇中性溶液也不變色,故當二者恰好完全反應后,再滴入一滴氫氧化鈉溶液時,燒杯中液體會由無色變紅色。
【數據處理】
解:設白醋中醋酸的質量分數為x%
CH3COOH + NaOH = CH3COONa + H2O
60 40
12ml×1g/ml×x% (45-5)ml×1g/ml×1.0%
60:40=(12ml×1g/ml×x%):[(45-5)ml×1g/ml×1.0%]
解得,x=5
由于標簽上注明醋酸的質量分數≥5%,從而判斷,這瓶白醋中醋酸的含量與標簽的標注相符。
答:白醋中醋酸的質量分數與標簽的標注相符。
考點:酸的化學性質,實驗探究物質的組成成分以及含量,化學實驗方案設計與評價
點評:解答這類題目時,要能根據問題情景,找到實驗探究的反應原理,以及計算所要用到的數據;再根據實驗的反應原理,利用所稱取的樣品進行實驗探究,分析推斷出該物質的組成成分;然后,再根據化學方程式計算出該樣品中某一成分的質量;最后,利用所求的該成分的質量,及所取樣品的質量求出所要探究的物質中該成分的含量。


科目:初中化學 來源: 題型:閱讀理解
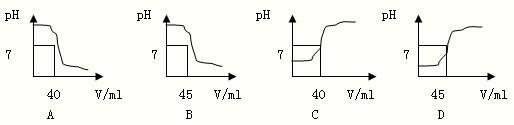
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
| 實驗操作 | 實驗現象 | 結論 |
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com