
 =
= =551(帕)
=551(帕)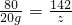
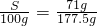


 全能測控一本好卷系列答案
全能測控一本好卷系列答案科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
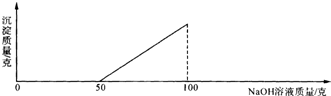
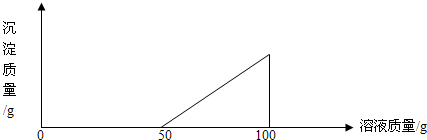
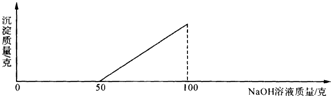
 在硫酸與硫酸銅的混合溶液200g中,滴入40%的氫氧化鈉溶液100g,恰好完全反應.記錄反應過程,得到的沉淀與所加的氫氧化鈉溶液的質量關系如圖所示.問:
在硫酸與硫酸銅的混合溶液200g中,滴入40%的氫氧化鈉溶液100g,恰好完全反應.記錄反應過程,得到的沉淀與所加的氫氧化鈉溶液的質量關系如圖所示.問:查看答案和解析>>
科目:初中化學 來源: 題型:
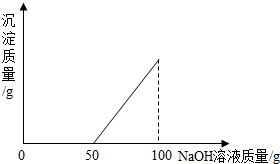
 在硫酸與硫酸銅的混合溶液200g中,滴入40%的氫氧化鈉溶液100g,恰好完全反應.記錄反應過程,得到的沉淀與所加的氫氧化鈉溶液的質量關系如圖所示.問:
在硫酸與硫酸銅的混合溶液200g中,滴入40%的氫氧化鈉溶液100g,恰好完全反應.記錄反應過程,得到的沉淀與所加的氫氧化鈉溶液的質量關系如圖所示.問:查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源:2009年黑龍江省中考化學模擬試卷(解析版) 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com