
分析 (1)碳酸鈣與鹽酸反應放出二氧化碳而使反應后質量減小,利用質量守恒定律可計算放出二氧化碳的質量;
(2)根據反應的化學方程式,由放出二氧化碳的質量計算蛋殼中所含碳酸鈣的質量.
解答 解:(1)根據質量守恒定律,產生二氧化碳的質量=6g+94g-97.8g=2.2g
故答案為:2.2;
(2)設6g該雞蛋殼中碳酸鈣的質量為x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2g
$\frac{100}{x}=\frac{44}{2.2g}$
x=5g
該雞蛋殼中碳酸鈣的質量分數:$\frac{5g}{6g}$×100%=83.3%.
答:該雞蛋殼中碳酸鈣的質量分數為83.3%.
點評 利用質量守恒定律求出反應放出二氧化碳的質量,是進行后面計算的基礎,體現出運用知識分析問題的能力.


科目:初中化學 來源: 題型:填空題

 .
.查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 α-丙氨酸是組成人體蛋白質的氨基酸之一,如圖是α-丙氨酸的分子結構模型圖,下列對α-丙氨酸的敘述正確的是( )
α-丙氨酸是組成人體蛋白質的氨基酸之一,如圖是α-丙氨酸的分子結構模型圖,下列對α-丙氨酸的敘述正確的是( )| A. | 由碳、氫、氧、氮四種原子構成 | B. | 氫元素的質量分數最大 | ||
| C. | 屬于氧化物 | D. | 化學式為C3H7O2N |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
 實驗室常用于制取氧氣的方法有:
實驗室常用于制取氧氣的方法有:查看答案和解析>>
科目:初中化學 來源: 題型:填空題
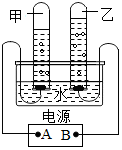 如圖是電解水實驗,試回答下列問題.
如圖是電解水實驗,試回答下列問題.查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 礦泉水、氧化鎂、空氣 | B. | 氮氣、過氧化氫、氯酸鉀 | ||
| C. | 木炭、水銀、牛奶 | D. | 紅磷、冰水、硬水 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com