
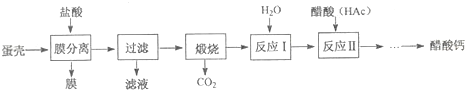
分析 (1)高溫條件下,碳酸鈣分解生成氧化鈣和二氧化碳;
二氧化碳在空氣中含量過高時會導致溫室效應;
根據反應的化學方程式可以判斷反應中CO2與CH4的最佳質量比;
(2)氫氧化鈣的溶解度很小;
氫氧化鈣屬于堿,可以用來中和酸性土壤;
(3)在反應II中醋酸過量能使氫氧化鈣完全反應;
氫氧化鈣和醋酸反應生成醋酸鈣和水;
(4)碳酸鈣和稀鹽酸反應生成氯化鈣、水和二氧化碳.
解答 解:(1)煅燒碳酸鈣生成氧化鈣和二氧化碳,反應的化學方程式為:CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaO+CO2↑;
CO2的任意排放會引發的環境問題是導致溫室效應;
將CO2與CH4一定條件下化合生成化工產品甲醛(HCHO)的化學方程式及其二氧化碳和甲烷的質量關系為:
CO2+CH4$\frac{\underline{\;一定條件\;}}{\;}$2HCHO,
44 16
則此反應中CO2與CH4的最佳質量比是:44:16=11:4.
故答案為:CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaO+CO2↑;溫室效應;11:4.
(2)在反應I中制備石灰乳,而不是制備澄清石灰水的目的是氫氧化鈣的溶解度很小,石灰乳中的氫氧化鈣含量比澄清石灰水中多,更利于提高醋酸鈣的產量;
熟石灰可以用來中和酸性土壤.
故填:氫氧化鈣的溶解度很小,石灰乳中的氫氧化鈣含量比澄清石灰水中多,更利于提高醋酸鈣的產量;中和酸性土壤.
(3)在反應II中醋酸過量能使氫氧化鈣完全反應;
反應II中,氫氧化鈣和醋酸反應生成醋酸鈣和水,反應的化學方程式為:Ca(OH)2+2HAc═Ca(Ac)2+2H2O.
故填:使氫氧化鈣完全反應;Ca(OH)2+2HAc═Ca(Ac)2+2H2O.
(4)膜分離時,鹽酸不能過量的主要原因是:加入鹽酸就是為了將蛋殼與膜分開,過量時會與碳酸鈣反應,會使制作醋酸鈣的原料減少.
故填:加入鹽酸就是為了將蛋殼與膜分開,過量時會與碳酸鈣反應,會使制作醋酸鈣的原料減少.
點評 合理設計實驗,科學地進行實驗、分析實驗,是得出正確實驗結論的前提,因此要學會設計實驗、進行實驗、分析實驗,為學好化學知識奠定基礎.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 用水除去氧化鈣中的碳酸鈣 | |
| B. | 用氯化鋇除去鹽酸中混有的稀硫酸 | |
| C. | 用鋅粒除去硫酸亞鐵中的硫酸銅 | |
| D. | 用氫氧化鋇除去碳酸鈉中混有的硫酸鈉 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

| 物質 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 溫度(℃) | 0 | 10 | 26 | 30 |
| 水溶液 | 7.31 | 9.28 | 11.03 | 12.98 |
| 氨(8%)溶液 | 1.41 | 1.58 | 2.25 | 3.36 |
| 氨(35%)溶液 | 0.44 | 0.75 | 0.82 | 非常壓 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
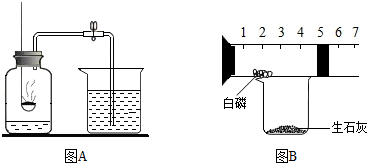
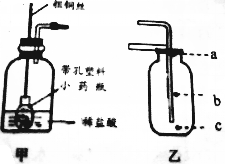 文文同學收集了一些家庭裝修時廢棄的大理石碎片,并查閱資料得知銅與稀硫酸、鹽酸不反應,鐵絲可以與稀硫酸和鹽酸反應.于是他設計了如圖的甲、乙兩裝置來制取二氧化碳,請回答下列問題:
文文同學收集了一些家庭裝修時廢棄的大理石碎片,并查閱資料得知銅與稀硫酸、鹽酸不反應,鐵絲可以與稀硫酸和鹽酸反應.于是他設計了如圖的甲、乙兩裝置來制取二氧化碳,請回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 將一定質量的Ca(OH)2溶液與Na2CO3溶液混合恰好完全反應,向反應后的混合物中加入稀鹽酸,產生氣體的體積與加入稀鹽酸的體積的關系如圖所示,下列說法中正確的是( )
將一定質量的Ca(OH)2溶液與Na2CO3溶液混合恰好完全反應,向反應后的混合物中加入稀鹽酸,產生氣體的體積與加入稀鹽酸的體積的關系如圖所示,下列說法中正確的是( )| A. | N點時,所得溶液中的溶質只有NaCl和HCl | |
| B. | M點時,所得溶液的pH>7 | |
| C. | OP段發生反應的化學方程式為Ca(OH)2+2HCl=CaCl2+2H2O | |
| D. | PM段發生反應的化學方程式為CaCO3+2HCl=CaCl2+H2O+CO2↑ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com