
 某同學(xué)家為解決水稻出現(xiàn)的病蟲害和倒伏問題,購買了一些鉀肥.該同學(xué)仔細看過鉀肥的包裝標(biāo)簽(如右圖所示)之后,對鉀肥中KCl的純度產(chǎn)生了興趣,于是他帶著鉀肥樣品到實驗室進行實驗,老師為其提供了相關(guān)的實驗用品.
某同學(xué)家為解決水稻出現(xiàn)的病蟲害和倒伏問題,購買了一些鉀肥.該同學(xué)仔細看過鉀肥的包裝標(biāo)簽(如右圖所示)之后,對鉀肥中KCl的純度產(chǎn)生了興趣,于是他帶著鉀肥樣品到實驗室進行實驗,老師為其提供了相關(guān)的實驗用品.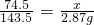 ,
, ×100%=93.13%,因93.13%>92%,
×100%=93.13%,因93.13%>92%,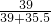 ×100%=0.78g,
×100%=0.78g, ×100%=48.75%,
×100%=48.75%,

科目:初中化學(xué) 來源: 題型:
 (2009?沈陽)某同學(xué)家為解決水稻出現(xiàn)的病蟲害和倒伏問題,購買了一些鉀肥.該同學(xué)仔細看過鉀肥的包裝標(biāo)簽(如右圖所示)之后,對鉀肥中KCl的純度產(chǎn)生了興趣,于是他帶著鉀肥樣品到實驗室進行實驗,老師為其提供了相關(guān)的實驗用品.
(2009?沈陽)某同學(xué)家為解決水稻出現(xiàn)的病蟲害和倒伏問題,購買了一些鉀肥.該同學(xué)仔細看過鉀肥的包裝標(biāo)簽(如右圖所示)之后,對鉀肥中KCl的純度產(chǎn)生了興趣,于是他帶著鉀肥樣品到實驗室進行實驗,老師為其提供了相關(guān)的實驗用品.查看答案和解析>>
科目:初中化學(xué) 來源:沈陽 題型:問答題

查看答案和解析>>
科目:初中化學(xué) 來源:2009年遼寧省沈陽市中考化學(xué)試卷(解析版) 題型:解答題

查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com