
分析 (1)根據氫氧化鈉的化學式和相對原子質量計算元素質量比;
(2)根據20℃時,NaCl的溶解度為36g進行分析;
(3)根據化學方程式和題中的數據進行計算.
解答 解:(1)NaOH中鈉、氧、氫元素的質量比為:23:16:1;
(2)20℃時,NaCl的溶解度為36g,所以飽和溶液中溶質和溶劑的質量比為:36g:100g=9:25;
(3)設生成H2的質量為x,生成Cl2的質量為y
2NaCl+2H2O═2NaOH+H2↑+Cl2↑
2×58.5 2 71
36g×32.5% x y
$\frac{117}{36g×32.5%}$=$\frac{2}{x}$=$\frac{71}{y}$
x=0.2g
y=7.1g
剩余溶液的質量=136g?0.2g?7.1g=128.7g,
答:剩余溶液的質量為128.7g.
故答案為:(1)23:16:1;
(2)9:25;
(3)剩余溶液的質量為128.7g.
點評 本題主要考查了化學方程式的計算,難度不大,注意解題的規范性和準確性.


 輕松課堂單元期中期末專題沖刺100分系列答案
輕松課堂單元期中期末專題沖刺100分系列答案科目:初中化學 來源: 題型:解答題
| 溫度/℃ | 0 | 40 | 80 |
| Ca(OH)2溶解度/g | 0.187 | 0.141 | 0.094 |
| Ba(OH)2溶解度/g | 1.67 | 8.22 | 101.4 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
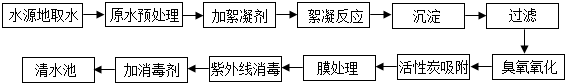
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
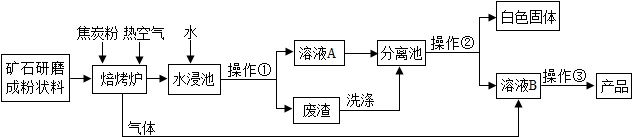
 純堿是一種重要的化工原料,廣泛應用于玻璃、造紙、紡織和洗滌劑的生產.
純堿是一種重要的化工原料,廣泛應用于玻璃、造紙、紡織和洗滌劑的生產. 所示.該氣體遇空氣中的水蒸氣易形成酸霧,腐蝕金屬設備.該酸霧腐蝕金屬鐵的化學方程式為Fe+2HCl═FeCl2+H2↑.
所示.該氣體遇空氣中的水蒸氣易形成酸霧,腐蝕金屬設備.該酸霧腐蝕金屬鐵的化學方程式為Fe+2HCl═FeCl2+H2↑.查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
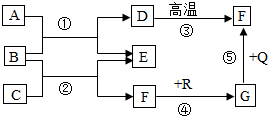 如圖是初中化學中常見物質間的轉化關系,其中,在通常情況下,F、G是組成元素相同的兩種氣體;Q、R都是黑色粉末;E是生活中常用的調味品(圖中“-”表示兩端的物質間能發生化學反應;“→”表示物質間存在轉化關系;部分反應條件和生成物略去).請回答:
如圖是初中化學中常見物質間的轉化關系,其中,在通常情況下,F、G是組成元素相同的兩種氣體;Q、R都是黑色粉末;E是生活中常用的調味品(圖中“-”表示兩端的物質間能發生化學反應;“→”表示物質間存在轉化關系;部分反應條件和生成物略去).請回答:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com